調査結果は、2018年5月10日、ジャーナル_cell_の発行に記載されています。
「この発見について本当にエキサイティングなのは、RNA依存性RNAポリメラーゼが非常に非効率的である理由を説明していることです」と、TSRI准教授のエリカ・オルマン・サフィアは言いました。 「この非効率性の分子基盤がわかったので、この弱さを活用してRNAウイルスの複製を完全に停止するために、薬物の設計を想像することができます。」
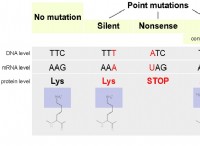
インフルエンザウイルス、エボラウイルス、ジカウイルスを含むRNAウイルスは、細胞の分子機械をハイジャックして自分自身のコピーを作成します。彼らがそうであるように、彼らはまったく同一ではない何千ものコピーを生成します。
この不正確さは、RNAウイルスの生存にとって非常に重要である、とサフィアによると、彼らは急速に進化することができるからです。また、インフルエンザなどの多くの人々に生涯にわたる免疫を獲得することを妨げます。
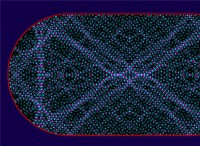
チームは、クリオエレクトロン顕微鏡を使用して、活動中の分子機械の画像をキャプチャすることにより、この発見をしました。彼らは、RNA依存性RNAポリメラーゼモーターが失速しやすいことを見ました。
モーターが失速すると、別の分子がプリを開き、動き続けるまで数秒間一時停止します。この「分子の綱引き」は、複製プロセスの非効率性を説明しています。
サフィアと彼女の同僚はまた、分子モーターが亜鉛原子に結合する小さなタンパク質構造である2つの亜鉛指によって調節されていることを発見しました。
「亜鉛指を遺伝的に変異させると、モーターはオーバードライブになり、複製プロセスが劇的に高速化されます」とサフィアは言いました。 「したがって、亜鉛の指は複製のブレーキとして作用しています。これは、それらが新薬の魅力的な標的になる可能性があることを示唆しています。」
薬物設計への影響
研究者は、RNAウイルスの亜鉛フィンガー調節因子をブロックする薬物は、これらのさまざまな病原体の効果的な治療法である可能性があると考えています。
「すべてのRNAウイルスを単一の薬物で標的にすることはできないと思いますが、特定の阻害剤でウイルスのファミリーを標的とすることができるかもしれません」とサフィアは言いました。 「それは、命を救い、パンデミックの脅威を減らすことができる広域スペクトル抗ウイルス薬を開発するための重要なステップになるでしょう。」
Saphireに加えて、「エボラウイルスRNA依存性RNAポリメラーゼのクリオエム構造」という論文の著者には、第一著者のマイケル・ロー、ジェシカ・タン、ニコラス・P・アンダーソン、ダニエル・I・スークップが含まれます。エリカ・N・オルソン、ロバート・P・ヘンダーソン、テキサス大学サウスウェスタン医療センターのクリストファー・B・バード。ペンシルベニア大学のマシュー・T・ドーガーティとデビッド・W・ハインツ。テキサス大学医療支部のカリッサ・A・ジョンソンとペイ・ヨン・シー。
この研究は、国立衛生研究所(GRANTS R01 AI121966、R01 AI120694およびR37 AI106547)、ウェルチ財団、防衛脅威削減機関、テキサスA&M患者研究所によってサポートされていました。