1。ホモリティック切断: 共有結合は、結合が破壊され、各原子が結合電子の1つを採取するホモリティック切断を受ける可能性があります。これは、結合が熱、光、または特定の化学試薬にさらされている場合に発生する可能性があります。たとえば、エタン(CH3-CH3)のC-C結合は、ホモリティック切断を受けて2つのメチルラジカル(CH3。)を形成することができます。
2。極性共有結合: 極性結合結合では、電子は原子間で均等に共有されません。これにより、部分料金の蓄積と債券の弱体化につながる可能性があります。たとえば、塩化水素(HCl)では、電子は塩素原子により強く引き付けられ、塩素に部分的な負電荷と水素に部分的な正電荷が得られます。この極性は、極性溶媒または他の分子による攻撃の影響を受けやすくなります。
3。立体効果: 原子または原子のグループが結合の周りに混雑すると、それらは立体障害を引き起こす可能性があり、それが結合を弱める可能性があります。たとえば、ネオペンタン(C(CH3)4)のような分子では、4つのメチル基が互いに非常に近く、有意な立体障害を生み出します。これにより、中央炭素とメチル基の間のC-C結合が弱くなる可能性があります。
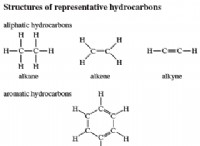
4。共鳴構造: 一部の分子には、分子内の電子の分布を表すさまざまな方法である複数の共鳴構造があります。共鳴構造が可能な場合、電子は複数の原子にわたって非局在化され、個々の共有結合を弱める可能性があります。たとえば、ベンゼン(C6H6)では、芳香環の電子は6つの炭素原子すべてにわたって非局在化されており、分子の安定性と強度に寄与します。
全体として、共有結合は一般に強力ですが、ホモリティック切断、極性、立体効果、共鳴などのさまざまな要因によって弱体化する可能性があります。共有結合の強度は、関与する特定の原子、それらの電気陰性度、分子の形状、および外部因子の存在に依存します。