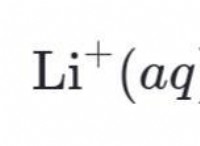CH3OH + H2O→CH3OH2 + + OH-
この反応では、メタノール分子は水分子にプロトン(H+)を寄付し、水素イオン(CH3OH2+)と水酸化物イオン(OH-)の形成をもたらします。ヒドロニウムイオンは本質的にプロトン化メタノール分子であり、水酸化物イオンは遊離ヒドロキシル基です。
メタノールが加水分解を受ける程度は、温度、酸触媒の濃度、および他の反応物または溶媒の存在など、いくつかの要因に依存します。通常の状態では、メタノールの加水分解は比較的遅い反応です。ただし、温度を上げるか、より強い酸触媒を使用することで加速することができます。
加水分解反応、ハイドロニウムイオン、および水酸化物イオンの産物は、溶液に存在する互いまたは他の反応物とさらに反応する可能性があります。たとえば、水酸化ナトリウム(NaOH)などの強力な塩基が存在する場合、水素イオンは水酸化物イオンと反応して水を形成しますが、メタノールは未熟成のままです。
CH3OH2 + + OH-→CH3OH + H2O
全体として、メタノールと水の間の反応は可逆プロセスであり、メタノール、ハイドロニウムイオン、および水酸化物イオンの間の平衡は、反応条件に応じてシフトできます。