1。電子構成: 鉄には比較的少数の原子価電子(最も外側の電子)があり、陽性イオン(陽イオン)を形成するために容易に失われます。これにより、他の要素、特に非金属と非常に反応します。対照的に、硫黄はより多くの価電子電子を持ち、電子を獲得して陰性イオン(アニオン)を形成する傾向があります。
2。金属結合: 鉄原子は、電子が非局在化し、構造全体で自由に移動する金属結合によってまとめられています。これにより、電気的および熱伝導性が高くなり、順応性と延性が可能になります。一方、硫黄は共有結合を形成し、そこでは電子が原子間で共有され、より脆くて導電性の低い構造につながります。
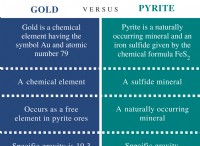
3。外観: 鉄は通常、光沢があり(光沢があります)、不透明、銀灰色が色があります。これらの特性は金属の特徴です。ただし、硫黄は黄色またはオレンジ色であり、鈍い非金属的な外観を持っています。
4。物理的特性: 鉄は、高融点、高密度、良好な引張強度など、金属に関連する特性を示します。硫黄は融点が低く、密度が低く、脆性です。
5。化学的特性: 鉄は酸素と容易に反応して、腐食の一般的な例である錆(酸化鉄)を形成します。また、酸と反応して水素ガスを形成します。 硫黄は金属と反応して硫化物を形成しますが、酸とは簡単に反応しません。
要約: 鉄と硫黄の重要な違いは、その電子構成と結果として生じる結合パターンにあります。 鉄の電子を失い、金属結合を形成する傾向は特徴的な金属特性を与え、硫黄の電子を獲得し、共有結合を形成することを好むことは、その非金属挙動につながります。