これが故障です:
* 銅イオン(Cu 2+ ) リチウムイオンよりも簡単に減少します(ゲイン電子)(li + )。
* リチウムイオン(li + ) 銅イオンよりも酸化されやすい(電子を失う)(cu 2+ )。
反応方程式:
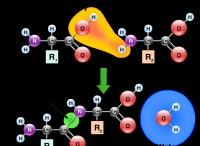
Cu 2+ (aq) + 2li(s)→cu(s) + 2li + (AQ)
説明:
* 銅イオン(Cu 2+ ) リチウム金属から2つの電子を獲得し、銅金属(Cu)になります 。
* リチウム金属(Li) 電子を失い、リチウムイオンになります(li + ) 。
観測:
* 赤茶色の銅金属 溶液から沈殿します。
*溶液は、残りのイオンの濃度に応じて色を変えます。
重要な注意: この反応は非常に発熱性です 、つまり、多くの熱を放出します。それは非常に活発である可能性があるため、制御された環境では注意して実行する必要があります。
追加情報:
*このタイプの反応は、変位反応として知られています 、より反応性のある金属(リチウム)が、その溶液からそれほど反応性の低い金属(銅)を変位させます。
*金属の反応性は、標準還元電位によって決定されます 。リチウムは銅よりもはるかに低い還元電位を持ち、電子を失い、酸化する可能性が高いことを示しています。