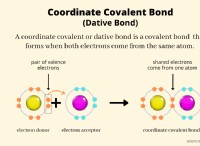
1。陽子と電子:
* 陽子: 原子核に位置する正に帯電した粒子。
* 電子: シェルまたはエネルギーレベルで核を周回する負に帯電した粒子。
2。ニュートラル電荷:
*中性原子では、プロトンの数(正電荷)は電子の数(負電荷)に等しくなります。
*この等しいバランスにより、正味電荷はゼロになり、原子は電気的に中立になります。
3。バランス法:
*原子はこの中立状態を維持するよう努めています。
*原子が電子を失ったり獲得したりすると、正味の正または負の電荷を運ぶイオンになります。
* カチオン: 電子を失う原子は、正に帯電したイオンになります。
* アニオン: 電子を獲得する原子は、負に帯電したイオンになります。
4。化学結合:
*原子は、多くの場合、他の原子と化学結合を形成することにより、安定したバランスのとれた状態を達成します。
*これらの結合には、電子の共有または伝達が含まれ、分子またはイオン化合物の形成につながることがあります。
例:
*ナトリウム原子(NA)には11個のプロトンと11個の電子があり、中性になります。
* +1電荷を運ぶナトリウムイオン(Na +)になるために1つの電子を失う可能性があります。
*塩素原子(CL)には17個のプロトンと17個の電子があり、また中性です。
* -1電荷を運ぶ塩化物イオン(CL-)になるために1つの電子を獲得できます。
*反対の電荷は引き付けられ、塩化ナトリウム(NaCl)にイオン結合を形成します - 一般的なテーブル塩。
要約:
原子は、同数のプロトンと電子を持つことにより、電荷バランスを維持します。このバランスは、化学的結合と物質の安定性にとって非常に重要です。原子が電子を獲得または失った場合、それはイオンになり、その電荷と反応性を変えます。