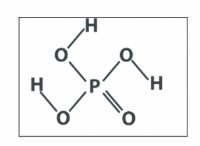
その理由は次のとおりです。
* 電子は、原子の最も外側のシェルを占有します(原子価シェル)。 これらの電子は、他の原子と相互作用する電子です。
* 化学結合は、原子間の電子の共有または伝達によって形成されます。 この共有または転送は、通常、完全な外側シェルを持つことにより、安定した電子構成を実現したい原子の欲求によって推進されます。
* 原子電子の数が原子の反応性を決定します。 ほぼ完全または空の外側のシェルを持つ原子はより反応性がありますが、完全な外側のシェルを持つ原子は反応性が低くなります。
陽子と中性子は原子(その原子数と質量)の同一性を定義するために重要ですが、それらは核に位置し、化学結合に直接関与していません。