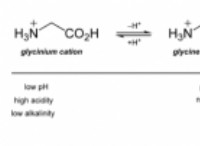
* 電解質: 塩化カリウムはイオン化合物です。水に溶けると、イオンに分離します:カリウムイオン(K+)と塩化物イオン(Cl-)。これらのイオンは、溶液全体で自由に移動できます。
* 電気伝導率: 物質が電気を導入するには、自由に移動できる荷電粒子が必要です。 塩化カリウム溶液中のこれらのモバイルイオンの存在により、電流の流れが可能になります。
それがどのように機能するか:
1。電圧が印加されている場合: 正のカリウムイオン(K+)は負の電極(カソード)に引き付けられ、負の塩化物イオン(Cl-)は正の電極(アノード)に引き付けられます。
2。電流フロー: 溶液を介したこれらのイオンの動きは、電流を構成します。
対照的に:
* 純水: 純水は、非常に少ないイオンを含むため、非常に貧弱な電気導体です。
* 非電解質: 砂糖(スクロース)のような物質は、水に溶解したときにイオンに解離しません。それらは中性分子としてのままであり、電気を導入することはできません。