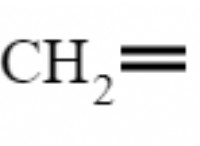* 分子内結合 分子内の強い化学結合 *です。 CL2の場合、これは2つの塩素原子間の共有結合です。これらの結合は、分子を一緒に保持する責任があり、非常に強力です。 CL2がガスから液体に移行すると変化しません。
* 分子間結合 *分子間の魅力 *の弱い力です。これらの力は、物質の物理的状態の原因です。 CL2では、主要な分子間力はロンドン分散力であり、分子の周りの電子分布の一時的な変動から生じます。
cl2が冷えるとき:
1.分子は運動エネルギーを失います。
2。より弱い分子間力は、より秩序ある配置でCl2分子を一緒に保持するのに十分な強さになり、液体状態を形成します。
要約: Cl2分子内の分子内結合は同じままですが、分子間の分子間力の強度は変化し、ガスから液体への移行を引き起こします。