その理由は次のとおりです。
* 価電子 原子の最も外側のエネルギーレベル(シェル)の電子です。これらの電子は、最もゆるく保持されている電子であり、他の原子と相互作用する最大の可能性があります。
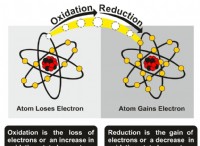
* 化学結合 原子間の電子の共有または伝達によって形成されます。
* 電子の共有 共有結合につながり、電子を伝達します イオン結合につながります。
たとえば、水分子(H₂O)では、各水素原子には1つの価電子があり、酸素原子には6つの価電子があります。 結合を形成するために、各水素原子はその価電子を酸素原子と共有し、2つの共有結合をもたらします。
そのため、要約すると、原子価は化学結合の重要なプレーヤーであり、原子がどのように相互作用して分子を形成するかを決定します。