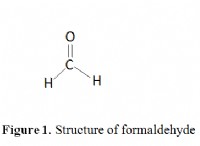
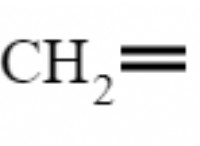1。酸化の程度: 原子が中性状態と比較して獲得または失われた電子の数を示しています。
* 陽性酸化数: 原子は電子を失いました。つまり、酸化されています。
* 負の酸化数: 原子は電子を獲得しました。つまり、縮小します。
* ゼロ酸化番号: 原子は電子を獲得したり失ったりしていません。
2。結合における原子の役割: 原子が化学結合にどのように関与しているかを理解するのに役立ちます。たとえば、正の酸化数は、原子が陽イオン(正に帯電したイオン)として作用していることを示すことがよくあり、イオン結合を形成します。
3。化学反応の予測: 酸化数は、化学方程式のバランスをとり、酸化還元反応の産物を予測するために重要です(電子の伝達を含む反応)。
4。化合物の性質の決定: その元素の酸化数が高い化合物は、多くの場合、非常に反応性または酸化剤です。
5。 化学物質の理解: 酸化数を使用して、化合物内の元素の化学的特性を予測できます。たとえば、酸化数が高い元素は一般に酸性ですが、酸化数が低い要素はより基本的です。
例を示します:
化合物 nacl を考えてみましょう (塩化ナトリウム)。
*ナトリウム(NA)の酸化数は+1です。これは、1つの電子を失ったことを意味します。
*塩素(Cl)の酸化数は-1です。これは、1つの電子を獲得したことを意味します。
この情報は、ナトリウムが酸化(電子を失った)し、塩素が減少したこと(電子を獲得)したことを示しています。この電子移動は、2つの要素間にイオン結合を形成し、化合物NaClを作成します。
全体として、酸化数は、分子内の原子の挙動と相互作用を理解するための強力なツールです。