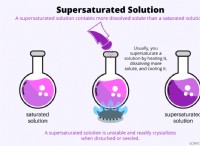
1。炭酸塩の式を決定します
どの炭酸塩を扱っているかを指定していません。粉ミル酸アンモニウムについて尋ねていると仮定しましょう。
2。炭酸アンモニウムのモル質量を計算します
*(nh₄)₂co₃=(2 * 14.01 g/mol(n)) +(8 * 1.01 g/mol(h)) +(12.01 g/mol(c)) +(3 * 16.00 g/mol(o)=96.09 g/molのモル質量
3。炭酸塩のグラムをほくろに変換します
*(nh₄)₂co₃=(8.903 g) /(96.09 g / mol)=0.0927 molのモル
4。アンモニウムイオンのモルを計算します
*式(nh₄)₂co₃から、1モルの炭酸アンモニウムごとに2モルのアンモニウムイオン(nh₄⁺)があることがわかります。
*nh₄⁺=(0.0927 mol(nh₄)₂co₃) *(2 molnh₄⁺ / 1 mol(nh₄)₂co₃)=0.1854 molnh₄⁺
したがって、8.903グラムの炭酸アンモニウムに約0.1854モルのアンモニウムイオンがあります。