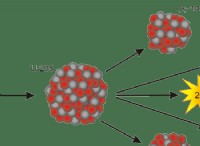
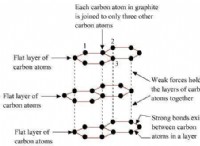
1。イオン結晶の構造:
* 固体状態: 固体状態では、イオン化合物は硬い結晶格子を形成します。イオンは、強力な静電力によって固定位置に保持されます。これは、電流を運ぶための自由移動帯電粒子がないことを意味します。
* 限定導電率: 一部のイオン固体は、構造の欠陥のためにわずかな導電率を示す可能性がありますが、一般的に非常に低いです。
2。水に溶ける:
* 極性: 水分子は極性です。つまり、正と負の端があります。
* 解離: イオン化合物が水に溶解すると、極水分子がイオンを囲み、それらを引き離します(解離)。水分子の正の端は陰性イオンを引き付け、水分子の負の端は正のイオンを引き付けます。
* 遊離イオン: イオンは、溶液中に独立して自由に動き回ることができます。
3。電気の伝導:
* モバイルチャージキャリア: 溶液中のこれらの自由移動イオンは、電荷キャリアとして作用します。溶液全体に電位(電圧)が適用されると、陽性イオンは負の電極に向かって移動し、陰性イオンは正の電極に向かって移動します。荷電粒子のこの動きは、電流を構成します。
要約:
*固体イオン化合物は、イオンが格子に固定されているため、電気を導入しません。
*水に溶解すると、イオンが自由になり、モバイルになり、電流を運ぶことができます。
重要な注意: 溶液中に電気を伝導するイオン化合物の能力は、水への溶解度に依存します。 化合物が溶解しない場合、そのイオンは自由に移動することはなく、導電率はありません。