コア コンセプト
トリカルボン酸回路またはクレブス回路としても知られるクエン酸回路は、生物が ATP を生成するために使用する異化好気性プロセスです。この記事では、クエン酸回路の 8 つの反応、それらの反応のしくみ、および関連する生成物と反応物について学びます。この記事では、クエン酸サイクル、トリカルボン酸サイクル (TCA)、およびクレブス サイクルという用語が同じ意味で使用されます。
他の記事で取り上げるトピック
- 解糖
- 酸化と還元
- 縮合反応
- 光合成
- E2
語彙
- 好気呼吸 - 酸素の存在下で炭水化物からエネルギーを生成するために使用される化学プロセス。
- 脱炭酸 – カルボキシル基の除去とその後の CO2 の放出 .
- デヒドロゲナーゼ - 電子の移動
- 水分子の水和付加
製品
- 3 NADH
- 2 CO2
- 1 FADH2
- 1GTP
注:各グルコースは 2 分子のアセチル CoA を生成します。したがって、リストされている製品は 2 倍にする必要があります。たとえば、2 分子のグルコースは次のものを生成します:
- 12 NADH
- 8 CO2
- 4 FADH2
- 4 GTP
上記の例は、生化学および細胞生物学のコースで一般的な試験問題です .
基板
- アセチルCoA
- クエン酸塩
- イソクエン酸
- α-ケトグルタル酸
- サクシニルCoA
- コハク酸
- フマル酸
- リンゴ酸
- オキサロ酢酸
酵素
- クエン酸合成酵素
- アコニターゼ
- イソクエン酸デヒドロゲナーゼ
- α-ケトグルタル酸デヒドロゲナーゼ
- サクシニルCoA合成酵素
- コハク酸デヒドロゲナーゼ
- フマラセ
- リンゴ酸デヒドロゲナーゼ
クレブス サイクルの紹介
クエン酸回路の目的は、アセチル CoA を二酸化炭素に酸化することによってエネルギーを生成することであり、他の生合成反応の前駆体として機能します。このプロセスは、ミトコンドリアのマトリックスで行われます。アセチルCoAのチオールエステル結合に蓄えられたエネルギーを捕捉し、後でそれをNADHのエネルギーパケットに保存します。酸素は消費されませんが、NADH と FADH2 から好気性サイクルになります。 電子を酸素依存経路に転送します。
ピルビン酸脱水素酵素複合体 – 準備段階
ピルビン酸は、ピルビン酸デヒドロゲナーゼ複合体を介してアセチル-CoAに合成されます。したがって、この多酵素複合体は、解糖をクレブス回路に結び付けます。 PDH複合体には、ピルビン酸デヒドロゲナーゼ(E1)、ジヒドロリポイルトランスアセチラーゼ(E2)、およびジヒドロリポイルデヒドロゲナーゼ(E3)の3つの酵素活性サブユニットがあります。重要なことに、ピルビン酸デヒドロゲナーゼにはアロステリック部位があり、その結果、ATP または NADH で調節できます。明らかに、このステップは、生物が ATP と AMP のレベルを評価できるようにするため、重要な制御形態です。
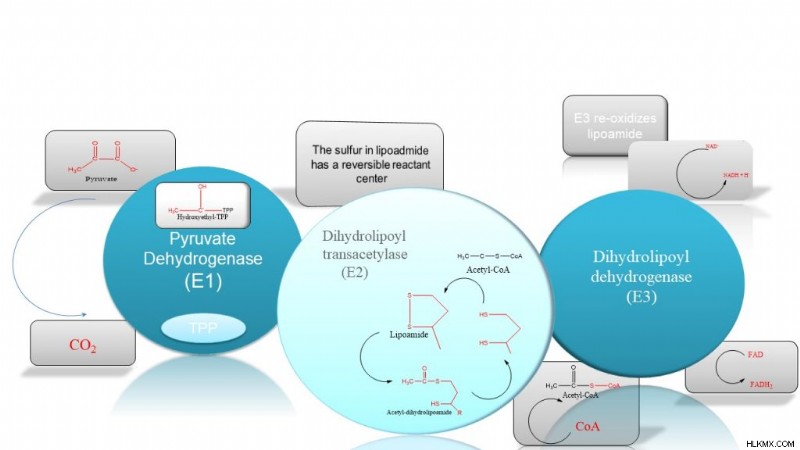
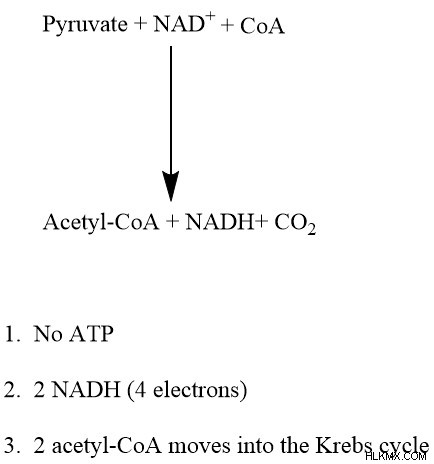
概要
| ポジティブモジュレーター | ネガティブモジュレーター |
| AMP | ATP |
| ADP | アセチル-CoA |
A. E1 の助けを借りて、ピルビン酸は酵素補因子であるチアミンピロリン酸 (TPP) と結合し、続いて脱炭酸を受けます。したがって、これによりヒドロキシエチル-TPP 中間体が形成されます。
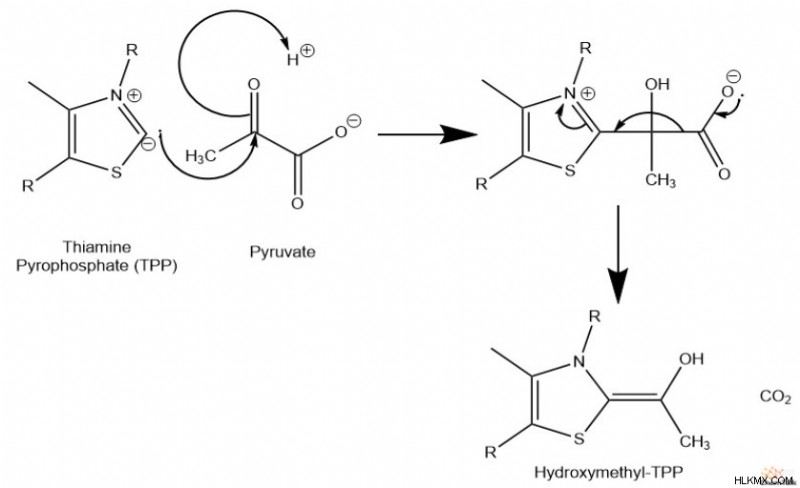
B. TPP のヒドロキシエチル基が E2 のリポアミドスルフィド基を攻撃し、TPP 誘導体を除去します。 TPP誘導体が放出されると、ヒドロキシエチルカルバニオンはアセチル基に酸化される。このステップでは、将来のピルビン酸削減のために TPP も再生されることに注意してください。
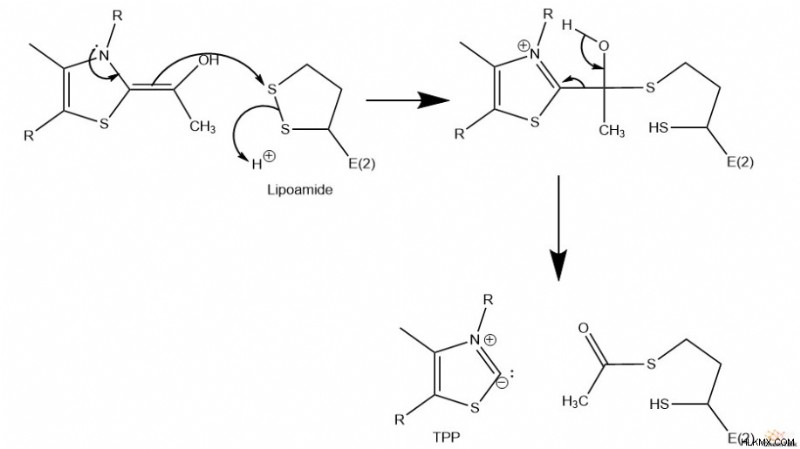
C. エステル交換の結果、アセチル基が CoA に転移し、アセチル CoA が生成されます。
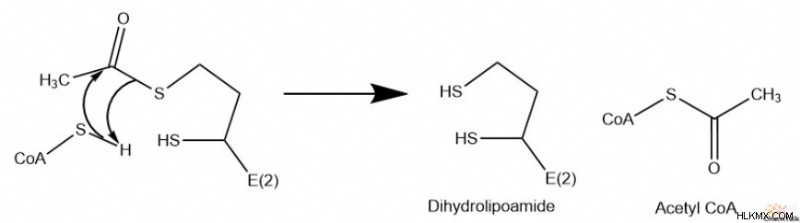
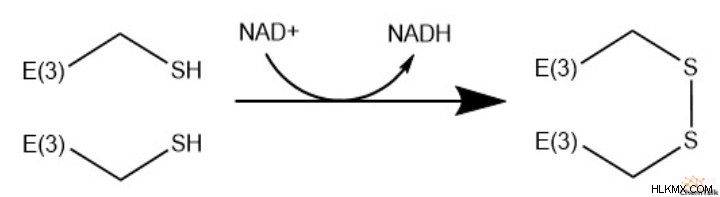
D. E3 はジヒドロリポアミドを再酸化して、E2 の元のリポアミド基を再生します。

E. 還元反応では電子の獲得があり、酸化では電子の喪失があることを思い出してください。この反応で E3 から失われた電子は、電子伝達系での ATP の生成を助ける NADH の生成を助けます。明らかなように、ピルビン酸デヒドロゲナーゼ複合体は ATP を直接生成しません。
クエン酸回路のステップ 1:クエン酸合成酵素/酸塩基反応
クエン酸合成酵素は、オキサロ酢酸と呼ばれる中間体とアセチル-CoA との間の反応を触媒して、後にクエン酸を形成します。このメカニズムは、アルドール縮合反応で始まり、チオエステル結合の加水分解で終わります。しかし、反応が起こる前に、シンターゼのヒスチジン 274 と 320 をプロトン化する必要がありますが、アスパラギン酸 375 は安静時に脱プロトン化されます。
メカニズム
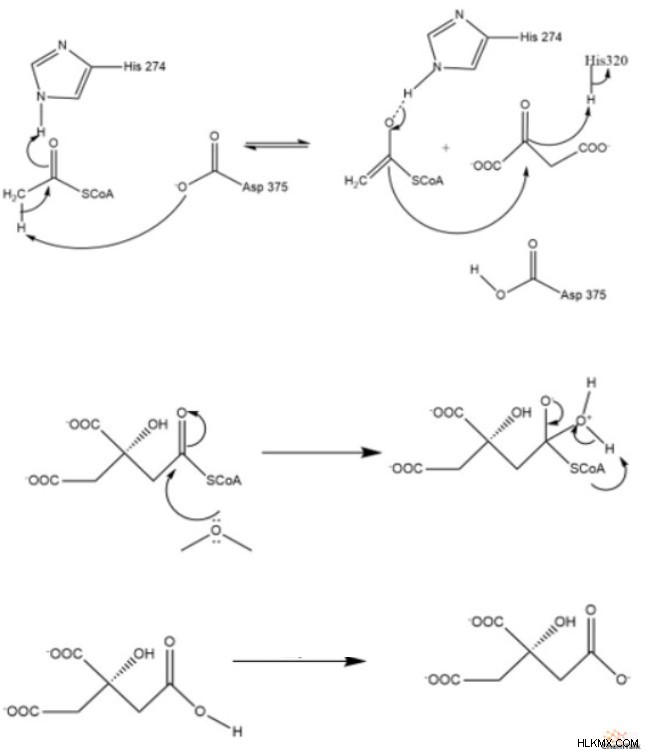
クエン酸回路 反応 2:アコニターゼ/脱水-再水和反応
アコニターゼは、cis-アコニターゼを介してクエン酸をその異性体であるイソクエン酸に相互変換する鉄硫黄酵素です。これは、水の追加とその後の除去を含む 2 段階のメカニズムです。
メカニズム
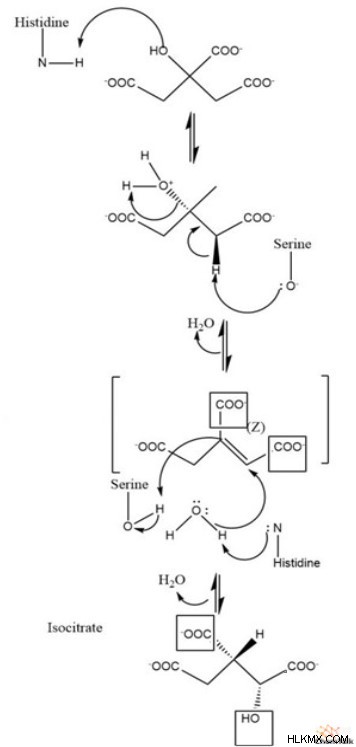
クエン酸回路 反応 3:イソクエン酸脱水素酵素/酸化的脱炭酸
イソクエン酸デヒドロゲナーゼは、イソクエン酸からその異性体であるα-ケトグルタル酸への酸化的脱炭酸を触媒する酵素です。これは重要な律速段階であるだけでなく、NADH と CO2 を放出するサイクルの最初の段階でもあります . Mgはエノラート中間体のカルボニルを安定化させ、最終的にα-ケトグルタル酸に変換します。重要なことに、このステップは、NADH または ATP の存在を考慮して、その後調整することができます。
メカニズム
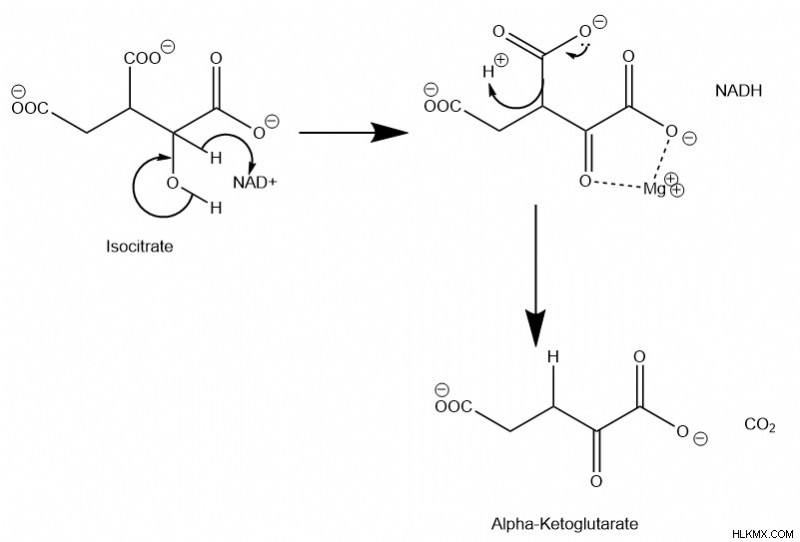
クエン酸回路 反応 4:α-ケトグルタル酸デヒドロゲナーゼ
α-ケトグルタル酸デヒドロゲナーゼは、酸化的脱炭酸によってα-ケトグルタル酸をスクシニル-CoAに変換する多酵素複合体です。さらに、この酵素は 2 番目の NADH と CO
メカニズム
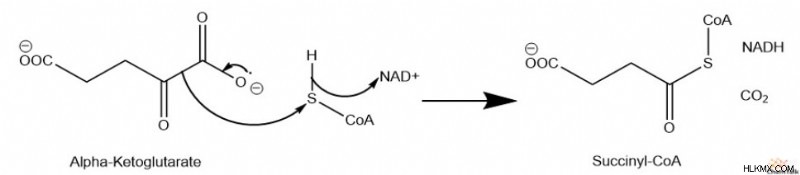
クエン酸回路 反応 5:スクシニル CoA 合成酵素 - 基質レベルのリン酸化。
スクシニル-CoA シンテターゼは、スクシニル-CoA の高エネルギー チオール エステルを切断してスクシネートを形成します。スクシニル-CoA のチオエステル結合から放出されたエネルギーは、GTP を生成するために使用され、GTP はそのリン酸を ADP に転移して ATP を生成します。ただし、リン酸はスクシニルリン酸から GTP に直接移動するのではなく、シンテターゼのヒスチジン残基を介して移動します。
メカニズム
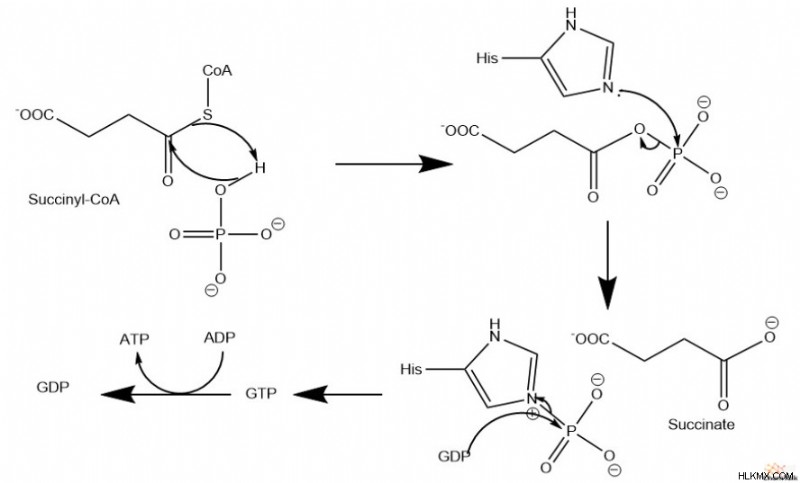
クエン酸回路 反応 6:コハク酸脱水素酵素/立体特異的脱水
コハク酸デヒドロゲナーゼは、コハク酸からフマル酸への脱水素反応を触媒します。この酵素は、ヒスチジン残基を介して共有結合している補欠分子族 FAD を含んでいます。コハク酸が酸化されると、2 つの水素原子が FAD に移動し、FADH2 が生成されます。 .コハク酸脱水素酵素は、トリカルボン酸回路の唯一の膜結合型酵素であり、電子伝達鎖に直接結合しています。
メカニズム
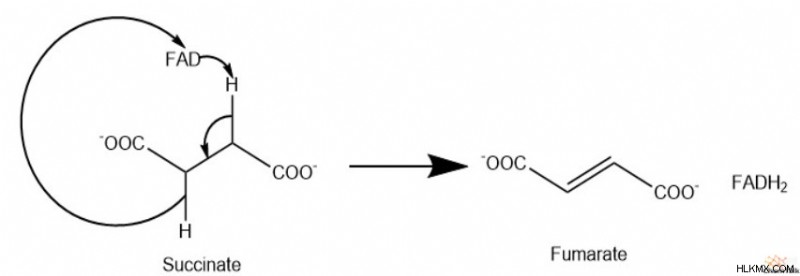
クエン酸回路 反応 7:フマラーゼ/水和反応
フマラーゼは、二重結合に水を付加してマレートを生成することにより、フマレートの水和反応を触媒します。
メカニズム
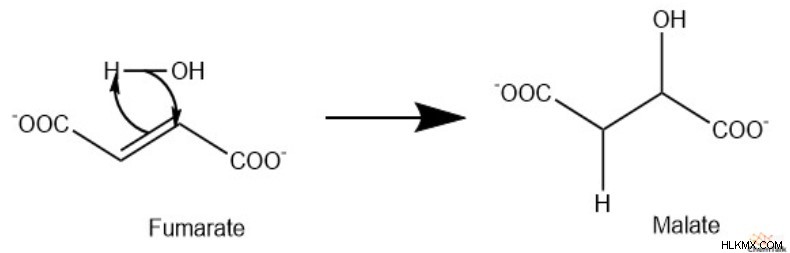
クエン酸回路 反応 8:リンゴ酸脱水素酵素
リンゴ酸デヒドロゲナーゼは、リンゴ酸のさらなる酸化と NAD+ の還元を結びつけます。これはカルボニルを形成し、リンゴ酸をオキサロ酢酸に変換し、最終的にクエン酸回路を完成させます.
メカニズム

クエン酸サイクルチートシート
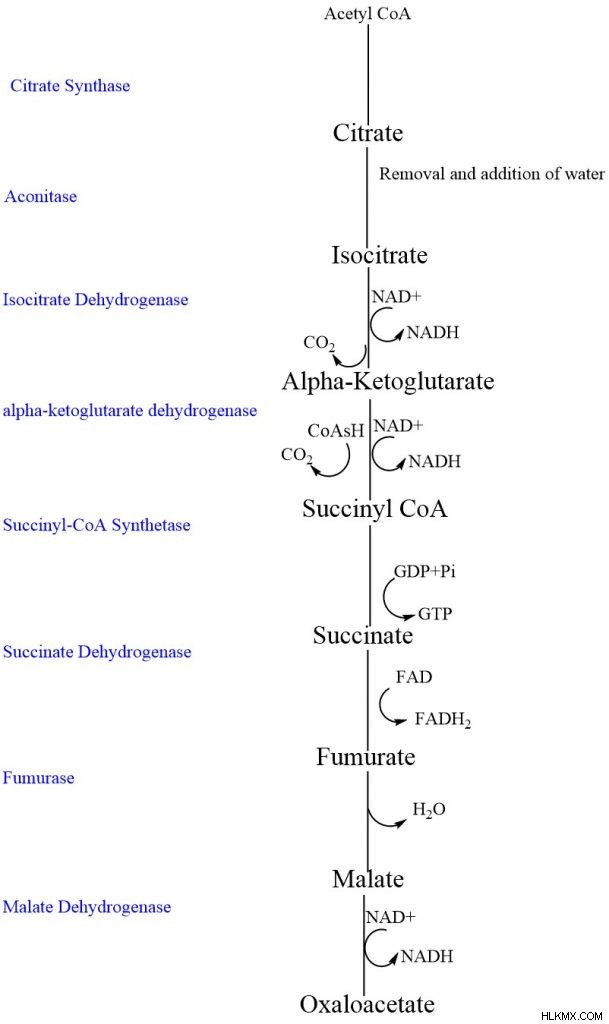
さらに読む
- がんにおけるTCA
- クレブス サイクルの重要性
- α-ケトグルタル酸の重要な役割