CuSO4 水溶液は、硫酸銅五水和物の化学式であり、CuSO4 と呼ばれます。水耕栽培や園芸用途で使用され、防腐剤や殺菌剤として使用され、プールの pH を下げるためにも使用されます.
CuSO4 溶液のエンタルピーは?
プロセスが一定の圧力下で発生する場合、吸収または放出される熱量はエンタルピーの変化に等しくなります。ただし、「エンタルピー」は魅力的でユニークな言葉であるため、ほとんどの人は、より頻繁に使用される「熱量」という用語の代わりに使用することを選択します。
エントロピーとエンタルピーはどちらもギリシャ語の「回転」に由来し、どちらも「温暖化」という用語に由来します。発音に関しては、エントロピーの最初の音節が強調されることが多く、エンタルピーの 2 番目の音節が通常強調されます。
CuSO4 の溶液のエンタルピーは -16 kcal で、CuSO4 のエンタルピーです。
溶解プロセス中に (一定圧力で) 放出または吸収される熱量を測定するため、溶液のエンタルピー変化と呼ばれます。
電気分解 CuSO4
電解質を水に溶かすと、電解質の原子はイオン結合によってしっかりと結合しているにもかかわらず、その分子は陽イオンと陰イオンに分解されます。プラスに帯電したイオンは陽イオンと呼ばれ、マイナスに帯電したイオンは陰イオンと呼ばれます。溶液中では、陽イオンと陰イオンの両方が自由に動き回ります。
CuSO4 としても知られる硫酸銅が水に導入されると、溶解します。
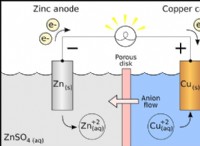
2 つの銅電極が溶液に浸されます。
Cu+ + イオン (カチオン) は、バッテリーのマイナス端子に取り付けられた電極であるカソードに引き寄せられます。各 Cu++ イオンは陰極から電子を受け取り、陰極に到達すると中性の銅原子になります。
同様に、SO4 (陰イオン) イオンは、バッテリーのプラス端に取り付けられた電極であるアノードに引き寄せられます。その結果、SO4 イオンはアノードに移動し、そこで 2 つの電子を放棄して SO4 ラジカルを形成します。
しかし、SO4 ラジカルは電気的に中性の状態では存在できないため、銅陽極を攻撃して硫酸銅を生成します。
電子を受け取った後、中性の銅原子が上記の手順でカソードに堆積します。同時に、SO4 は銅陽極と相互作用して CuSO4 を形成しますが、水中では単一の分子として存在することはできないため、CuSO4 は Cu++ と SO4 に分裂し、水に溶解します。
その結果、銅電極を使用した CuSO4 の電解中に銅がカソードに析出し、同量の銅がアノードから除去されます。硫酸銅電解中に銅または他の金属電極の代わりに炭素電極を使用すると、電解反応が多少変化します。 SO4 は炭素と結合できないため、溶液中の水と反応して硫酸を生成し、酸素を放出します。
電気分解は、上記の手順を表す用語です。
CuSO4 水溶液
CuSO4 水溶液は本質的に酸性です。これは、硫酸銅が水に溶解し、化学反応を起こして酸性になるためです。 CuSO4 (s) + 2H2O =CuOH2l + H2SO4 (aq) CuSO4 (s) + 2H2O =CuOH2l + H2SO4 (aq) 上記の化学式からわかるように、生成された硫酸は強い鉱酸であり、酸性度を引き起こします。上昇するソリューションの。
結論
CuSO4 の溶液のエンタルピーは 16 kcal です。電気分解は、イオン化された電解質溶液内で電流が 1 つの電極から次の電極に流れる電気化学的プロセスです。陽イオンまたは陽イオンは陰極または陰極に引き寄せられ、陰イオンまたは陰イオンは陽極または陽極に引き寄せられます。