簡単に言えば、水素結合は水素結合の形成です。それは主に電気陰性と水素原子の間で発生します。一般的な電気陰性原子には、フッ素、塩素、および酸素があります。共有結合またはイオン結合と比較して、水素結合は一般的に弱いです。ただし、ファンデルワールス力よりは強い。専門家は、水素結合を弱い化学結合の一種として分類しました。
水素結合の条件をテーマに、水素結合と水素結合を形成するためのさまざまな条件について、関連トピックとともに詳しく学びます。
水素結合について説明する
水素結合は、水素原子と非常に電気陰性度の高い原子との間の相互作用によって生じる分子間引力の特別なクラスである水素結合を形成するプロセスとして説明できます。たとえば、水分子の場合、化学的には H2O と表され、水素は電気陰性度の酸素原子に共有結合しています。
その結果、酸素原子と水素原子の間の双極子間相互作用により、水分子の水素結合が上昇します。専門家によると、通常の分散や双極子間力と比較すると、水素結合はほとんど強力です。ただし、イオン結合や真の共有結合と比較すると弱いようです。さらに、水素結合は大きく2つに分けられます。
分子間水素結合は、同じまたは異なる化合物を持つ異なる分子間で起こる水素結合の一種です。
分子内水素結合は、主に分子内でのみ発生する別のタイプの水素結合です。このタイプの水素結合は、2 つのグループを持つ化合物で発生します。
水素結合の条件
原子が電気陰性原子に密接に結合している分子では、電子の共有部分が引き付けられます。その結果、分子の末端はわずかにマイナスに見えますが、他の部分はプラスになります。両端が互いに引き付け合い、弱い結合が形成されます。説明した結合は、水素結合と呼ばれます。
水素結合のため、1 つの水素原子は同時に 2 つの電気陰性原子に密接に結合します。 2つのうち、1つは共有結合に接続されています。もう一つは水素結合によるものです。水素結合の 2 つの主な条件は次のとおりです。
電気陰性原子のサイズは小さくなければなりません。電気陰性原子のサイズが小さくなるほど、静電引力は大きくなります。
各分子には、水素原子に接続された非常に電気陰性度の原子が必要です。電気陰性度が高いほど、分子の分極が高くなります。
水素結合のため、カルボン酸分子は暗く見えます。そのようなすべての化合物のセルグループは、2 倍の大きさです。
水素結合の例
水素結合の最も一般的な例のリストを以下に示します –
<オール>水中の水素結合
水分子には、水素原子に結合した電気陰性の酸素原子があります。酸素原子は電子の共有ペアを引き付ける傾向があるため、その端は負になります。ただし、水素原子はプラスになります。
-
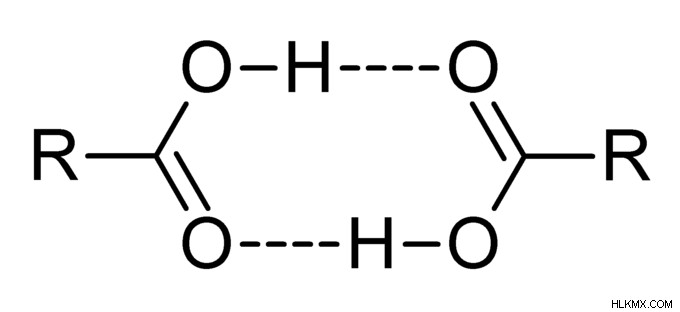
カルボン酸とアルコールの水素結合
アルコールは、-OH 基を持つ有機分子と呼ばれます。一般に、水素原子を持つ分子が窒素または酸素に直接結合している場合。その後、水素結合が容易になります。
-
フッ化水素の水素結合
フッ素は電気陰性度が最も高いため、最も強い水素結合が形成されます。
H-F···H-F···H−F
-
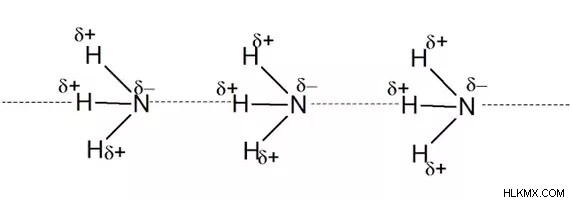
アンモニア中の水素結合
水素原子に結合した電気陰性原子の窒素があります。
-
ポリマー中の水素結合
天然および合成タンパク質が獲得した特性と立体構造を決定するために、水素結合は重要な要素です。また、亜麻や綿などの派生ポリマーとともにセルロース構造を定義する上でも重要な役割を果たします。

水素結合を持つ化合物は沸点と融点が高いですか?
水素結合化合物は、一般に非常に高い融点と沸点を示します。これは、結合を切断するのにより多くのエネルギーが必要になるためです。水素結合が存在するため、ハロゲン酸間の沸点は一般的に高いです。
結論
水素結合は水素結合を形成するプロセスです。水素結合は、水素原子と非常に電気陰性度の高い原子との間の双極子間相互作用によって生じる分子間引力の特別なクラスです。専門家は、水素結合を弱い化学結合の一種として分類しました。それは主に電気陰性と水素原子の間で発生します。
水素結合の一般的な例としては、フッ化水素の水素結合、水中の水素結合、アンモニアの水素結合、ポリマーの水素結合などがあります。水素結合の形成には主に3つの条件があり、それについて詳しく説明しました。後半では、水素結合を持つ化合物が高沸点・高融点を示す理由についても説明しました。これが、水素結合の条件をよりよく理解するのに役立つことを願っています.