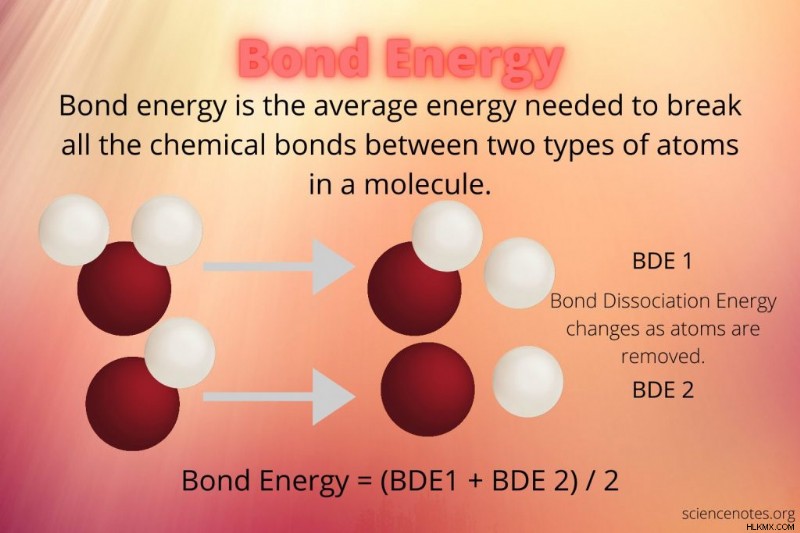
絆エネルギー (BE) は、分子内の同じ 2 種類の原子 (炭素と水素、水素と酸素など) 間のすべての化学結合を切断するのに必要なエネルギーの平均量です。平均結合エンタルピーまたは平均結合エンタルピーとも呼ばれます。典型的な単位は、1 モルあたりのキロカロリー (kcal/mol) または 1 モルあたりのキロジュール (kJ/mol) です。結合エネルギーは、化学結合の結合強度の尺度です。
結合エネルギーと結合解離エネルギーの違い
結合エネルギーと結合解離エネルギーは関連する概念です。結合エネルギーは、分子内の単一タイプの結合のすべての結合解離エネルギーの平均です。
結合解離エネルギーは結合の種類 (C-H、O-H、O=O など) の一定値であると考えるかもしれませんが、実際には各化学結合が切断されると変化します。分子の残りの部分の組成も、結合解離エネルギー値に影響します。
たとえば、水中の O-H の結合解離エネルギー (H2 O) は、最初の結合が切断された場合と、2 番目の結合が切断された場合とで異なります。結合エネルギーはこれらの値の平均です。
結合エネルギーは、分子内の特定の結合 (例:O-H) の単一の値ですが、結合解離エネルギーは、それが最初に壊れた結合であるかどうか、および化合物の残りの部分で何が起こっているかによって変化する可能性があります。
結合解離値の表は、ホモリティックな結合切断に関するものであることに注意してください。これが意味することは、結合に参加している電子は、結合が壊れたときに製品間で均等に分割されるということです。実際には、一部の結合はヘテロリティックに切断され、共有された電子は一方の製品に移動し、他方の製品には移動しません。これは、遷移金属と一部の配位子で発生します。
絆エネルギーと絆の強さの関係
大きな結合エネルギー値は、強力な化学結合と安定した分子を示します。高い結合エネルギーは、共有結合に関与する 2 つの原子間の短い距離と相関します。結合エネルギーの値が小さい場合は、化学結合が比較的弱く、分子の安定性が低いことを示します。結合エネルギーが小さい場合、2 つの原子間の距離が大きくなります。したがって、化学結合内の 2 つの原子間の距離がわかれば、結合エネルギーを予測できます。また、短い結合は二重結合または三重結合になる傾向があり、長い結合は単結合になります。
イオンはしばしば格子状に配置されるため、イオン化合物では少し異なります。距離は、絆の強さの指標として信頼できるものではありません。結合エネルギーは、2 つの原子の電気陰性度の値の差が大きくなるにつれて増加します。言い換えると、電気陰性度の差が大きい原子間で最も強いイオン結合が形成されます。
結合が壊れたり形成されたりすると、エネルギーが放出されますか?
化学結合を切断するには、常にエネルギーの入力が必要です。結合は、原子が分離できるようにエネルギーを吸収します。結合破壊は吸熱プロセスです。その値には常に正の符号があります。
化学結合を形成すると、常にエネルギーが放出されます。結合形成は発熱プロセスです。そのエンタルピー変化は負です。
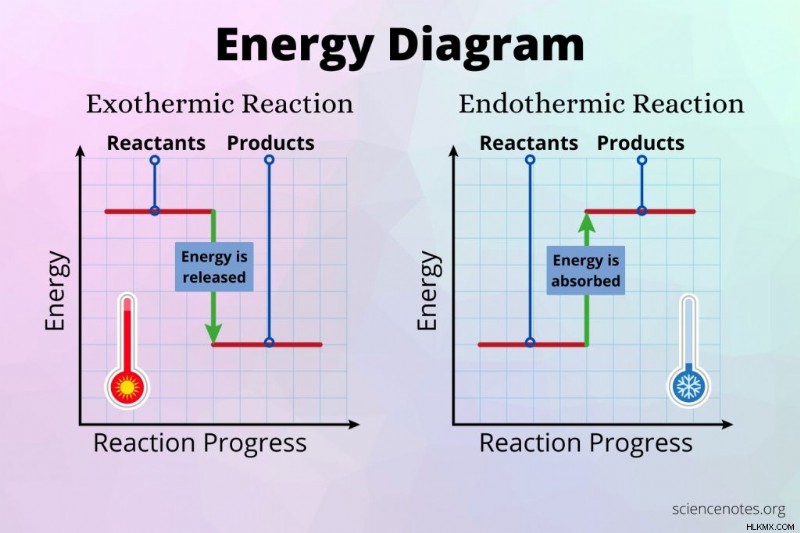
化学反応が発熱性であるか吸熱性であるかは、結合を切断するために吸収されるエネルギーと、新しい結合を形成するために放出されるエネルギーとの差によって決まります。結合の切断が結合形成の放出よりも少ないエネルギーを吸収する場合、反応は発熱です。結合の切断が結合形成の解放よりも多くのエネルギーを吸収する場合、反応は吸熱反応です。







