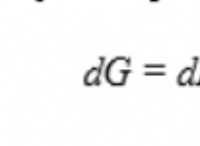アルドール反応は、新しい C-C 結合を形成する最もよく知られたプロセスの 1 つであり、化学合成と生物学の両方の分野で応用されています。従来のアルドール反応では、望ましい結果を得るために、水性アルコール媒体で塩基性触媒を使用するか、有毒で可燃性の有機溶媒で強塩基を使用する必要がありました。延長された反応時間の結果として、そのような条件は、ケトールと不飽和ケトンの組み合わせ、競合する副反応からの副生成物、およびアルドール生成物、ならびに単独のアルドール生成物を生成する。過去数年間、環境に優しい環境でこの変換を行うための触媒法の開発に多大な努力と関心が向けられてきました。より良い結果を達成するために、いくつかの均一および不均一触媒タイプが調査されているという事実にもかかわらず、触媒アルドールプロセスに関連する環境問題があります。環境意識と環境に優しい反応の重要性が高まるにつれて、化学者は、とりわけ従来のアルドール縮合法の代替として、ミセル媒体、マイクロ波照射、超音波などの高度な方法論を採用し始めました。このレビューでは、環境に配慮した観点からこれらのルートに関する研究を分析および更新しており、アクセスしやすいスタイルで書かれています。不均一系触媒を使用するかどうかに関係なく、これらの技術の下で行われる反応は、前述のように、グリーンケミストリーの原則に従って強調されています。プロトコルは主に教育ジャーナルから編集されており、環境に優しいものにするために、適切な場合は常に環境に配慮した構成要素が描かれています。
アルドール縮合反応
アルドール縮合は、エノラート イオンがカルボニル化合物と結合してヒドロキシ ケトンまたはヒドロキシ アルデヒドを生成し、その後脱水されて反応の結果として共役エノンを生成する化学プロセスとして特徴付けることができます。アルドール縮合反応は、炭素-炭素結合の形成経路を提供するため、有機合成において重要です。
アルドール反応はこのプロセスの最初の要素であり、脱水 - 脱離反応は 2 番目の要素です (これには水またはアルコール分子の除去が含まれます)。活性なカルボキシル基が存在する場合、脱水の後に脱炭酸が続く可能性があります。求電子機構では、カリウム t-ブトキシド、水酸化カリウム、水素化ナトリウムなどの強塩基を使用してアルドール付加生成物を脱水できますが、酸触媒エノール機構では酸を使用できます。アルドール縮合は、一般に動力学的制御と熱力学的制御の 2 種類の状況下で行うことができます。どの条件が使用されるかは、対象製品の性質によって決まります。
アプリケーション
アルドール縮合反応は、次の種類の合成反応に利用できます:
<オール>交差アルドール縮合
架橋アルドール反応は、水やアルコールなどの非プロトン性溶媒中でのアルデヒドまたはケトンの 2 つの異なる分子の縮合です。 「交差アルドール縮合」という語句は、2 つの別個のカルボニル化合物間で起こる縮合を指します。両方のアルデヒドがアルファ水素を含む場合、それらはカルバニオン受容体としても機能しながら、カルバニオンを生成することができます。その結果、合成価値が限られた 4 つの化学物質の非効率的な組み合わせが生成されます。
アルデヒドの 1 つがアルファ水素を含まない場合、それはカルバニオン受容体としてのみ機能します。この状況では、生成される生成物は 2 つだけです。交差アルドール反応を行う場合、α位を持たない芳香族アルデヒドが頻繁に使用される基質です。最初の縮合生成物の脱水は迅速に行われ、その結果、α-不飽和ケトンが合成され、結果としてレトロアルドール反応の発生が防止されます。
分子内アルドール縮合
内部アルドール縮合は、より有利であるため、分子間アルドール縮合よりも好ましい。環化は、最初のカルボニル炭素原子と 2 番目のカルボニル炭素原子が共有結合を形成することによって 5 員環または 6 員環を形成できる場合に発生します。これらのリングが 2 つ以上の反応で生成される可能性がある場合は、どちらの手順が有利かを判断する必要があります。平衡条件下では、多くの潜在的なエノラートが低濃度で多様な形態で存在します。その結果、より優れた求核剤であるエノラートが、より反応性の高いカルボニル炭素原子を攻撃し、生成された生成物の大部分を引き継ぎます。ケトンのカルボニル炭素原子へのエノラートの付加よりも、一般化された分子内アルドール縮合 (アルデヒドがエノラートによって攻撃されるものなど) が優先されます。
結論
アルドール縮合は新しい C-C 結合を生成できるため、最も重要な化学反応の 1 つですが、この反応のメカニズムは完全には理解されていません。ベンズアルデヒドとアセトフェノンとの塩基触媒アルドール縮合における水酸化物の最後の損失と C-C 結合の生成は、カルコンの形成をもたらし、プロセスの律速段階であると結論付けました。中間ケトールの分配比と溶媒速度論的同位体効果の調査結果によると、実験で使用された置換基に関係なく、縮合は H2O よりも D2O でより迅速に発生します。