その理由は次のとおりです。
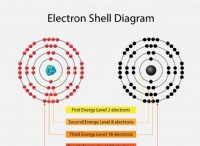
* 価電子 原子の最も外側のエネルギーレベルの電子です。彼らは化学結合に関与しているものです。
* nobleガス それらはすでに電子の完全な外側のシェルを持っているため、非常に反応性のない要素のグループであり、安定した構成を与えます。
* オクテットルール: ほとんどの原子は、多くの場合、電子を獲得、紛失、または共有して8つの原子価電子を持つことにより、貴族のような安定した構成を実現するよう努めています。
貴族の例:
*ヘリウム(彼)-2価電子(オクテットルールの例外)
* Neon(NE)-8価電子
* Argon(AR)-8価電子
*クリプトン(KR)-8価電子
* xenon(xe)-8価電子
*ラドン(RN)-8価電子
これらの概念のいずれかについてもっと情報をご希望の場合はお知らせください!