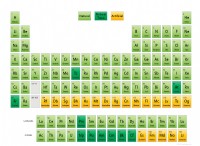
* 非金属原子: 非金属原子は電気的に中性です。同数のプロトン(正電荷)と電子(負電荷)があります。
* アニオン: 陰イオンは負に帯電したイオンです。 1つ以上の電子を獲得しており、陽子よりも多くの電子を獲得しています。
これが故障です:
非金属原子
* 例: 塩素原子(CL)
* 構造: 17陽子と17個の電子
* チャージ: ニュートラル(0)
anion
* 例: 塩化物イオン(cl⁻)
* 構造: 17個の陽子と18個の電子
* チャージ: -1(1つの余分な電子)
なぜ非金属は陰イオンを形成するのですか?
非金属は、安定した電子構成を実現するために電子を獲得する傾向があります(通常は完全な外側シェル)。これは、それらが電気陰性であるため、電子に強い魅力を持っているためです。
要約:
非金属原子とその陰イオンの違いは、単に陰イオンに1つ以上の電子を添加することです。電子の数のこの変化は、原子の全体的な電荷を変化させ、それを負にします。