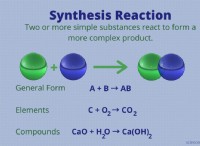
* 共有結合: HClは室温でガスとして存在します。水素と塩素原子は共有結合し、電子を共有します。これは、電流を運ぶための自由移動帯電粒子(イオン)がないことを意味します。
ただし、HClが水に溶解すると(塩酸を形成する)、電気の優れた導体になります :
* イオン化: HCl分子は水と反応し、水素イオン(H+)および塩化物イオン(CL-)に分解されます。
`` `
Hcl(g) + h2o(l)→H3o +(aq) + cl-(aq)
`` `
* 遊離イオン: 充電された粒子であるこれらの遊離イオンの存在により、電気が溶液を流れるようになります。正に帯電した水素イオンは、負の電極(カソード)に向かって移動し、負に帯電した塩化物イオンは正の電極(アノード)に向かって移動します。
要約:
*気体HClは導体が不十分です 遊離イオンがないからです。
*水性HCl(塩酸)は良好な導体です それがイオン化されるため、電流を運ぶ遊離イオンを生成します。