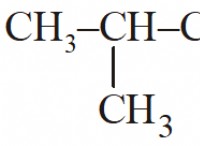価電子電子の数が炭素の結合にどのように影響するかは次のとおりです。
* 共有結合: 炭素の4つの価電子は、共有結合を容易に形成することを可能にします 、他の原子と電子を共有します。この共有は、複雑な分子を構築するために不可欠な強力な結合を生み出します。
* 4つの結合: 炭素は通常、4つの共有結合を形成します 。これは介して可能です:
* 単一結合: 1つの電子を別の原子と共有します。
* 二重結合: 別の原子と2つの電子を共有します。
* トリプルボンド: 別の原子と3つの電子を共有します。
* 多様な構造: シングル、ダブル、トリプルの結合を形成する能力と、それ自体と結合する能力(カテネーション)により、カーボンは信じられないほどの構造を形成することができます。これには次のものが含まれます。
* 線形チェーン: メタン(CH4)のようなアルカンで見つかった。
* 分岐チェーン: イソブタン(C4H10)のような分岐アルカンに見られる。
* リング: シクロヘキサン(C6H12)のような環状化合物に見られる。
* 複雑な3D構造: タンパク質、炭水化物、およびその他の高分子に見られる。
要約すると、炭素の4つの価電子は、共有結合の膨大な配列を形成することができる多用途の要素になり、有機分子の驚くべき多様性と複雑さをもたらします。