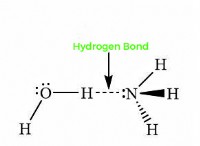
* イオン結合: イオン結合は、電気陰性度の大きな違いを持つ元素間に形成されます。 1つの元素(通常は金属)は電子を失い、正の帯電イオン(陽イオン)になり、もう1つの元素(通常は非金属)が電子をゲインして負に帯電したイオン(アニオン)になります。
* フッ素: フッ素は最も電気陰性の要素です。これは、電子を強く引き付けることを意味します。
* 金属と非金属: 金属は電子を失い、陽イオンを形成する傾向がありますが、非金属は電子を獲得して陰イオンを形成する傾向があります。
したがって、フッ素とイオン化合物を形成する可能性が最も高い元素は金属です。
例:
* ナトリウム(Na): ナトリウムは、1つの電子を容易に失い、+1カチオン(Na +)を形成する金属です。 フッ素はこの電子を獲得して-1アニオン(f-)を形成します。これらのイオンは結合してフッ化ナトリウム(NAF)を形成します。
* カルシウム(CA): カルシウムは、2つの電子を容易に失い、+2陽イオンを形成する金属です(Ca +2)。フッ素は1つの電子を獲得しますが、カルシウムは2つを失うため、電荷のバランスをとるために2つのフッ化物イオンが必要です。これにより、フッ化物カルシウム(CAF2)が形成されます。
キーテイクアウト: フッ素とのイオン結合形成を検討するときに、陽イオン(金属)を容易に形成する元素を探します。