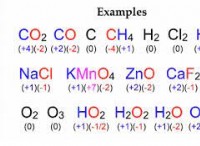
塩化ナトリウム(NaCl)
* イオン化合物: 塩化ナトリウムはイオン化合物であり、積極的に帯電したナトリウムイオン(Na+)と負に帯電した塩化物イオン(CL-)の間の静電引力によって形成されます。この強い魅力は、非常に安定した構造を作成します。
* オクテットルール: ナトリウムと塩素の両方が、電子を獲得または失うことにより、安定した電子構成を実現します。ナトリウムは1つの電子を失い、Na+になり、塩素は1つの電子を獲得してCl-になります。この安定した構成により、さらに反応する可能性が低くなります。
* 高格子エネルギー: 塩化ナトリウムのイオン間の強い引力は、高い格子エネルギーをもたらします。つまり、イオン間の結合を破るには多くのエネルギーが必要です。
塩素(cl 2 )
* 珪藻分子: 塩素は二原子分子として存在します(Cl 2 )、つまり、2つの塩素原子が結合していることを意味します。この結合は、塩化ナトリウムのイオン結合と比較して比較的弱いです。
* 電子親和性: 塩素は電子親和性が高いため、安定した電子構成を実現するために電子を容易に獲得します。
* 酸化剤: 塩素は強力な酸化剤であるため、他の物質から電子を容易に受け入れ、非常に反応性があります。
要約:
* 塩化ナトリウムは、その強いイオン結合、安定した電子構成、および高い格子エネルギーのために安定しています。 それは本質的に「満足している」化合物です。
* 塩素は、その弱い珪藻結合、高い電子親和性、および酸化剤として作用する能力のために反応性があります。 電子を獲得し、他の要素と安定した結合を形成しようとしています。
他に化学の質問がある場合はお知らせください!