その理由は次のとおりです。
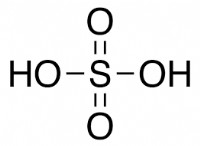
* 中央原子: 硫黄は中心原子です。
* 価電子: 硫黄には6つの価電子があり、各水素原子には1つの原子価があります。
* 結合: 硫黄は、2つの水素原子と2つの単一結合を形成します。
* 孤立ペア: 硫黄には、2つの孤立した電子ペアがあります。
* 電子ペア反発: 硫黄の2つの孤独なペアは結合ペアを撃退し、水素原子を近くに押し込み、曲がった形を作ります。
H₂Sの結合角は約 92°です 、孤立ペアの反発が大きいため、109.5°の理想的な四面体角度よりもわずかに小さいです。