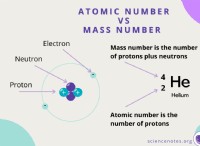
* 原子はニュートラルです: 原子には、同数のプロトン(正の帯電した粒子)と電子(負に帯電した粒子)があります。このバランスは、ニュートラルな全体的な電荷をもたらします。
* イオンが充電されます: イオンは、電子を獲得または失った原子または分子であり、正味の電荷を与えます。
* 陽性イオン(陽イオン): 原子が電子を *失うと、電子よりも多くの陽子があります。この過剰な正電荷により、原子は陽イオンとも呼ばれる正の帯電イオンになります。
例: ナトリウム(Na)には11個の陽子と11個の電子があります。正のイオン(Na +)になると、1つの電子が失われ、11個のプロトンと10個の電子が残り、+1電荷が発生します。
キーテイクアウト:
*電子を失うと、正電荷が生じます。
*原子の陽子の数はその原子数を決定し、一定のままです。
*原子がイオンを形成すると、電子の数が変化します。