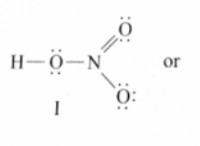
ただし、アンモニアは水と反応してアンモニウムイオン(nh₄⁺)を形成できます およびヒドロキシドイオン(OH⁻) 、イオン種です。
これが反応の方程式です:
nh₃(aq) +h₂o(l)⇌nh₄⁺(aq) +oh⁻(aq)
これは平衡反応です 水中のアンモニアのイオン化のため。二重矢印は、反応が両方向に進行できることを示しています。
キーポイント:
*アンモニアは弱い塩基であり、水で部分的にしかイオン化しないことを意味します。
*反応は可逆的であり、反応物と生成物の相対濃度は溶液のpHに依存します。
したがって、アンモニアのイオン方程式は、特定の反応と他の種の存在に依存します。