1。水素欠乏:
* 理論的飽和: 6つの炭素を備えた完全に飽和炭化水素には、式C 6 があります。 h 14 (一般式c n に従います h 2n+2 )。
* ベンゼンの式: ベンゼンには式C 6 があります h 6 、つまり、水素原子が4つ少ない 飽和6炭素化合物よりも。この「水素欠乏」は、不飽和の特徴です。
2。反応性:
* 添加反応: 比較的反応性のない飽和炭化水素(アルカン)とは異なり、ベンゼンは *置換反応 *を受けます。ここで、水素原子は別の原子またはグループに置き換えられます。これは、リングシステムの電子が典型的な二重結合よりも非局在し、より安定しているためです。
* 水素化: ベンゼンは水素化を強制され、環に水素原子を加え、非局在化システムを破壊することができます。これには、かなりのエネルギーと圧力が必要であり、さらに不飽和性を示しています。
3。分子構造:
* 非局在電子: リング内の6つの電子は、典型的な二重結合のような特定の炭素原子の間に局在していません。代わりに、それらは非局在化されており、リングの平面の上と下に雲を形成します。この非局在化は、その安定性に貢献しますが、反応のための電子の可用性も示しています。
4。分光証拠:
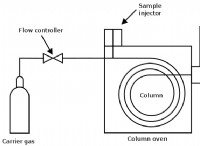
* NMR分光法: ベンゼン中の水素原子の化学シフトは、芳香族環の特徴であり、電子の非局在化を示しています。
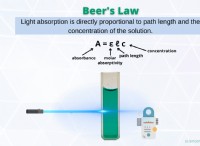
* UV-vis分光法: ベンゼンは、非局在化したPI電子のために紫外線を吸収します。これは、その不飽和性のもう1つの兆候です。
要約: ベンゼンの構造は従来の二重結合を示していませんが、その水素欠乏、反応性、非局在電子、および分光特性はすべて、それが不飽和化合物であることを確認しています。 「アロマティック」という用語は、このユニークなタイプの不飽和を説明するために使用されます。