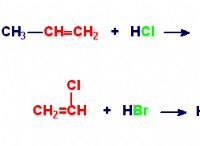
1。バランスの取れた化学式を書きます:
na₂co₃(aq) +cacl₂•2h₂o(aq)→caco₃(s) + 2nacl(aq) +2h₂o(l)
2。モル質量を計算します:
*na₂co₃:(2 * 22.99) + 12.01 +(3 * 16.00)=105.99 g/mol
*CACL₂•2H₂O:40.08 +(2 * 35.45) +(2 * 18.02)=147.02 g/mol
3。質量をモルに変換:
*na₂co₃のモル:1.00 g / 105.99 g / mol =0.00943 mol
*cacl₂oのモル•2h₂o:1.00 g / 147.02 g / mol =0.00680 mol
4。制限反応物を決定します:
* バランスの取れた方程式のモル比を使用: 方程式は、Na₂co₃とcacl₂•2h₂oの間の1:1モル比を示しています。
* モールを比較: caCl₂(0.00943 mol)よりも2H₂O(0.00680 mol)のモルが少ないため、cacl₂•2H₂oは制限反応物です。
説明:
制限反応物は、最初に完全に消費される反応物であり、反応がさらに進行するのを防ぎます。この場合、より多くのモルがna₂co₃を持っていますが、すべてのcacl₂•2h₂oが使用されると反応が止まります。