* 構造: 有機酸には通常、カルボキシル基(-COOH)が含まれています。このグループは、プロトン(H+)を溶液に寄付し、酸性にすることができます。ただし、カルボキシル基内のC-O結合は比較的強いため、プロトンは簡単に放出されません。
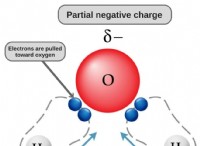
* 誘導効果: 有機酸のカルボキシル基に付着した炭素鎖の電子吸引性の性質は、O-H結合から電子密度を引き離すことにより、酸性度をわずかに増加させることができます。しかし、この効果は一般に、カルボキシル基の酸素の強い電気陰性度よりも弱く、比較的弱い酸につながります。
* 共鳴安定化: プロトンを寄付した後に形成されたカルボキシレートアニオン(COO-)は、共鳴によって安定化されます。この電子の非局在化により、陰イオンがより安定しますが、酸を別のプロトンを寄付する可能性が低くなるため、その弱さに貢献します。
例:
* 酢酸(CH3COOH) - 酢に含まれる最も一般的な有機酸は弱酸です。
* ギ酸(HCOOH) - アリの刺し傷で見つかりました、それは弱酸です。
* クエン酸(C6H8O7) - 柑橘類に見られるのは、弱酸です。
強酸 一方、溶液中に陽子を容易に寄付します。例には、塩酸(HCl)と硫酸(H2SO4)が含まれます。
重要な注意: シュウ酸などの一部の有機酸は、他の有機酸よりもわずかに強いです。ただし、一般に、有機酸は、その構造と上記の因子のために弱酸と見なされます。