関係を理解する
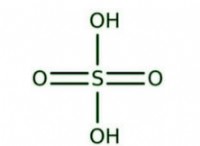
* ホウ酸(h₃bo₃): ホウ素を導入するために使用する化合物。
* boron(b): ソリューションに必要な要素。
計算
1。モル質量:
*ホウ酸(h₃bo₃):61.83 g/mol
*ホウ素(b):10.81 g/mol
2。ホウ酸のホウ素率:
*(10.81 g/mol b)/(61.83 g/molh₃bo₃)x 100%=17.48%
3。比:
* 1%のホウ素溶液を取得するには、ホウ酸を17.48倍に希釈する必要があります。
4。ホウ酸の量:
* 100 gの溶液ごとに、17.48 gのホウ酸が必要です。
例:
1%のホウ素溶液の1リットル(1000 g)を作成するには、次のことが必要です。
*(1000 g溶液)/(100 g溶液/17.48 gホウ酸)= 174.8 gのホウ酸
重要なメモ:
* 溶解度: ホウ酸の水への溶解度は限られています。溶解度の制限を確認して、1%のホウ素濃度を達成できるようにします。
* 安全性: ホウ酸は弱酸です。化学物質を扱うときは常に適切な安全装置を着用し、適切な実験室の慣行に従ってください。
* アプリケーション: 農業、木材保存、一部の産業プロセスなど、さまざまな用途で1%のホウ素溶液が使用されています。
別の体積またはホウ素濃度のホウ酸の量を計算したい場合はお知らせください。