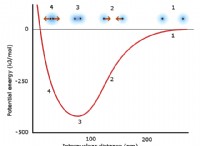
これらの2つのイオンが互いに近づくと、反対の電荷が強く引き付けられ、イオン結合が形成されます 。この魅力により、塩化リチウム(LICL)が形成されます。 化合物。
プロセスの内訳は次のとおりです。
1。電子伝達: 1つの価電子を備えたリチウムは、安定した電子構成を実現するためにこの電子を容易に失います。 7つの原子価電子を備えた塩素は、オクテットを完成させるために電子を容易に獲得します。
2。イオン結合形成: 陽性に帯電したリチウムイオン(li⁺)と負に帯電した塩化物イオン(Cl⁻)は、静電力のために互いに引き付けられます。この引力はイオン結合を形成し、中性化合物を作成します。
3。塩化リチウム(LICL): 得られた化合物は、白い結晶性固体である塩化リチウムです。 li⁺とcl⁻の間のイオン結合は強く、安定した溶解性化合物につながります。
要約すると、リチウムによる電子の損失と塩素による電子の獲得は、互いに引き付ける反対に帯電したイオンを生成し、安定したイオン化合物である塩化リチウムを形成します。