その理由は次のとおりです。
* 化学式: hc₂h₃o₂は、酢の主要成分である酢酸の化学式です。
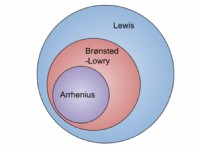
* 解離: 弱酸は水中で部分的にのみ解離します。つまり、イオンに完全に分解しないことを意味します(h⁺およびc₂h₃o₂⁻)。 これは、溶液が同じ濃度の強酸よりもH⁺イオンの濃度が低いことを意味します。
* 平衡: 弱酸の解離は平衡反応であり、酸分子が常に形成され、改革されていることを意味します。この均衡は、酸のない形態を好みます。
対照的に、強酸は水で完全に解離し、高濃度のh⁺イオンをもたらします。