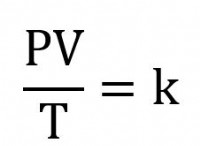1。活性化エネルギーと反応速度:
* 活性化エネルギー: 化学反応は、活性化エネルギーと呼ばれる一定量のエネルギーを開始する必要があります。 このエネルギーは、反応物内の既存の結合を破るために必要であり、新しい結合が製品を形成して作成できるようにします。
* 熱エネルギーの役割: 熱はこの活性化エネルギーを提供します。 分子が熱を吸収すると、それらは振動してより速く移動し、活性化障壁を克服するのに十分なエネルギーとの衝突の可能性を高めます。これにより、反応速度が高速化されます。
2。吸熱および発熱反応:
* 吸熱反応: これらの反応吸収 周囲から熱。 製品は、反応物よりも高いポテンシャルエネルギーを持っています。これは、熱エネルギーが結合を破り、新しいものを形成するために吸収されることを意味します。例は、光合成であり、植物は日光を吸収してグルコースを作り出します。
* 発熱反応: これらの反応放出 周囲に熱します。製品は、反応物よりもポテンシャルエネルギーが低いです。これは、結合が形成されると熱エネルギーが放出されることを意味します。一般的な例は、燃焼が熱を放出する燃焼です。
3。平衡と温度:
* 平衡: ほとんどの化学反応は可逆的であるため、両方向に進むことができます。平衡状態では、前方反応と逆反応の速度が等しくなります。
* 温度の衝撃: 温度を変更すると、平衡点がシフトできます。温度を上げると、変化に対抗するために吸熱反応(吸収熱)が有利になります。逆に、温度を下げると発熱反応が促進されます(熱の放出)。
4。例:
* 料理: コンロまたはオーブンからの熱は、食物分子を分解するための活性化エネルギーを提供し、それらが反応して構造を変えることができます。
* 爆発: これらには、非常に迅速な発熱反応が含まれ、大量の熱とエネルギーを放出します。
* 生物における化学反応: 酵素、生物学的触媒、活性化エネルギーを低下させることにより、多くの場合微妙な熱変動を通じて反応を高速化します。
要約:
熱エネルギーは、活性化エネルギーに影響を与え、反応が吸熱性であるか発熱性であるかを決定することにより、化学反応に基本的な役割を果たし、平衡状態に影響を与えます。このエネルギーは、外部から(溶液の加熱など)供給したり、反応自体で生成されたりできます。この関係を理解することは、さまざまな用途での化学反応を制御および予測するために不可欠です。