1。既知の酸化番号を割り当てます:
* 水素(H): +1(水素化物を除く)
* 酸素(O): -2(過酸化物とスーパーオキシドを除く)
2。方程式を設定します:
ニュートラル化合物の酸化数の合計は、ゼロに等しくなければなりません。
2(+1) + 2(x) + 8(-2)=0
どこ:
* +1は水素の酸化数です
* xは硫黄の酸化数です
* -2は酸素数です
3。 x:を解決します
* 2 + 2x -16 =0
* 2x =14
* x =+7
したがって、h₂s₂o₈の硫黄の酸化数は+7です。
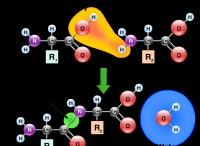
重要な注意: これは、通常-2〜 +6の範囲であるため、硫黄にとってはかなり珍しい酸化状態です。ペルオキシジスルフル酸とも呼ばれるH₂S₂O₈におけるペルオキシ結合(O-O)の存在は、この高い酸化状態の原因です。