1。固体状態:
*その固体状態では、NaClは結晶格子として存在します。ナトリウム(Na+)および塩化物(Cl-)イオンは、強力な静電力によって固定位置にしっかりと保持されます。
*この固定配置により、イオンが自由に移動するのを防ぎ、固体NaClを電気の導体が貧弱にします。
2。溶融状態:
* NaClがその融点まで加熱されると、イオンを保持する静電力が弱くなります。
*イオンは固定位置から解放され、モバイルになります。これらのモバイルイオンは電流を運ぶことができるようになり、溶融naClが良好な導体になります。
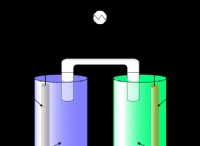
3。ソリューション状態:
* NaClが水に溶けると、水分子がイオンを囲み、互いに分離します。
*水和と呼ばれるこのプロセスは、イオン間の静電引力を弱め、自由に移動できるようにします。
*その後、水分補給イオンは溶液全体に移動し、電流を運び、溶液を良好な導体にします。
要約:
塩化ナトリウムは、イオンが自由に移動して電流を運ぶことができるため、溶融または溶液中の電気を伝導します。 イオンの可動性は、電気伝導率にとって重要です。