これが故障です:
基本:
* 滴定: 既知の濃度(滴定剤)の溶液が、反応が完了するまで未知の濃度(分析対象物)の溶液にゆっくりと追加されるプロセス。
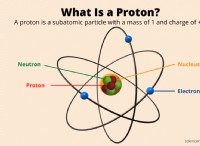
* 酸塩基反応: 反応には酸とベースが含まれ、酸はプロトン(H+)を寄付し、ベースがそれを受け入れます。この反応は中和と呼ばれます 。
それがどのように機能するか:
1。準備: 分析物の既知の体積(不明濃度)がフラスコに入れられます。ブレットには滴定剤(既知の濃度)が満たされています。
2。滴定: 滴定剤は、絶えず攪拌されながら、ゆっくりと分析物に加えられます。
3。エンドポイント: 滴定剤の追加は、反応がニュートラルな点に達するまで続き、エンドポイント 。これは通常、ソリューションに追加されたインジケーターの色の変化によって示されます。
4。計算: エンドポイントに到達するために使用される滴定剤の体積が測定されます。この体積は、抑制性の既知の濃度とともに、化学量論を使用して分析物の濃度を計算するために使用されます。
重要なコンポーネント:
* 滴定: 分析物との反応に使用される既知の濃度の溶液。
* 分析物: 未知の濃度の解。
* インジケーター: エンドポイントで色を変える物質で、反応が完全であることを示します。
* ブレット: 滴定を正確に供給するために使用される、停留所のあるグラッジガラスチューブ。
アプリケーション:
酸塩基の滴定は、さまざまな分野で広く使用されています。
* 化学: 酸と塩基の濃度を決定する。
* 食品科学: 食品の酸性度の分析。
* 医薬品産業: 薬物と製剤の純度を決定します。
* 環境監視: 水サンプルの酸性度を分析します。
簡単に言えば: 酸塩基の滴定は、希望の味が得られるまで、レシピに既知の量の成分を追加するようなものです。追加した金額を測定することにより、レシピに元の成分がどれだけであったかを把握できます。