反応物を理解する:
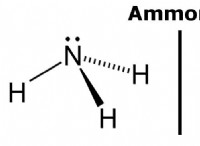
* NH4OH(水酸化アンモニウム): これは弱いbaseです。 アンモニア(NH3)および水(H2O)との平衡状態に存在します。
NH4OH⇌NH3 + H2O
* H2SO4(硫酸): これは強酸です。
反応:
水酸化アンモニウム(NH4OH)が硫酸(H2SO4)と反応すると、次の反応が発生します。
2 NH4OH + H2SO4→(NH4)2SO4 + 2 H2O
説明:
* 酸塩基中和: この反応には、酸(H2SO4)から塩基(NH4OH)へのプロトン(H+)の移動が含まれます。
* 塩形成: この反応は、塩分である硫酸アンモニウム((NH4)2SO4)を形成します。これは塩です。
* 水層: 水は反応の副産物として生成されます。
二重変位ではない理由:
二重変位反応には、2つの反応物間のイオンの交換が含まれます。 この場合、反応にはプロトン(H+)の移動が含まれますが、これは典型的なイオンの交換ではありません。
キーポイント: NH4OHとH2SO4の間の反応は、二重変位反応ではなく、酸塩基中和反応です。