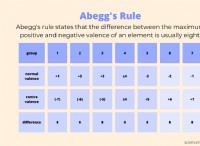
その理由は次のとおりです。
* 電気陰性度: ホウ素の電気陰性度は2.04、ヨウ素の電気陰性度は2.66です。電気陰性度(0.62)の違いは、結合をイオン性として分類するのに十分な大きさではありません。
* 電子の共有: 1つの原子が電子を他の原子に完全に伝達する代わりに、ホウ素とヨウ素は電子を共有して安定した電子構成を実現します。この電子の共有は、共有結合を形成します。
結合は共有結合と見なされますが、電気陰性度の違いは極性共有特性を持つことを示唆していることに注意することが重要です 、ヨウ素原子にわずかに負の電荷があり、ホウ素原子はわずかに正電荷を有しています。