固体中の伝導:
* イオン構造: 塩化カリウムはイオン化合物であり、積極的に帯電したカリウムイオン(K+)と負に帯電した塩化物イオン(CL-)の間の静電引力によって形成されます。
* 固定位置: 固体状態では、これらのイオンは、硬い結晶格子構造に配置されています。それらは固定位置に保持され、自由に移動することができません。
* 電荷キャリアなし: イオンは固定されているため、電流を輸送するモバイル電荷キャリアはありません。
液体中の伝導(溶融状態):
* 融解およびイオンの動き: 塩化カリウムが溶けると、格子内にイオンを保持する強力な静電力が克服されます。イオンは自由に壊れてモバイルになります。
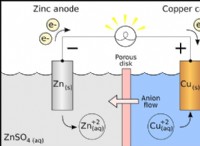
* 無料電荷キャリア: これらの現在のモバイルイオンは、電荷キャリアとして作用できます。 溶融KCl全体に電位が適用されると、正のカリウムイオンは負の電極(カソード)に向かって移動し、負の塩化物イオンは正の電極(アノード)に向かって移動します。イオンのこの動きは、電流の流れを構成します。
要約:
* ソリッドKCl: イオンは固定されており、電荷キャリアなし、伝導なし。
* Molten KCl: イオンはモバイルであり、電荷キャリアとして機能し、電気を行います。