その理由は次のとおりです。
* 電気陰性度: これらの要素は電気陰性度が高いため、電子に強い魅力があります。
* 電子構成: それらは、ほぼ外側の電子殻を満たしているため、安定した高貴なガス構成を実現するために、さらに少数の電子が必要です。
電子を獲得することにより、これらの要素はより安定した電子構成を実現できるため、より安定して反応性が低下します。
例:
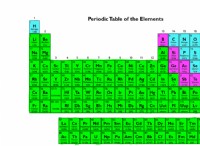
* グループ16(カルコジェン): 酸素(O)、硫黄(S)、セレン(SE)、テルリウム(TE)、ポロニウム(PO)
* グループ17(ハロゲン): フッ素(F)、塩素(CL)、臭素(BR)、ヨウ素(I)、アスタチン(AT)
これらの要素は一般に電子を獲得しますが、原子の特定の挙動は、化学反応に関与する他の要素を含む状況に依存することに注意することが重要です。