1。アンモニアの性質:
* 弱いベース: アンモニア(nh₃)は弱い底です。これは、溶液中に水酸化物イオン(OH⁻)を容易に寄付しないことを意味します。
* ガス状の状態: 純粋で気体状態では、アンモニアはリトマスの紙と相互作用し、その基本的な性質を示すために必要な条件を持っていません。
2。溶媒としての水:
* 加水分解: アンモニアが水に溶けると、加水分解と呼ばれる可逆反応が起こります。
* nh₃(g) +h₂o(l)⇌nh₄⁺(aq) +oh⁻(aq)
* 水酸化物イオン: この反応は、アンモニウムイオン(NH₄⁺)と水酸化物イオン(OH⁻)を産生します。
* 基本的な文字: 溶液を基本的にするのは、これらの水酸化物イオンの存在です。
3。 Litmus Paperの応答:
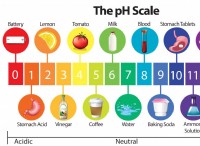
* 酸性条件: Litmusの紙は、酸性溶液(高いH⁺濃度)で赤くなります。
* 基本条件: Litmus Paperは、基本的なソリューションで青くなります(高いOH⁻濃度)。
* 乾燥アンモニア対水性アンモニア: 乾燥アンモニアは水酸化物イオンを産生しないため、リトマスの紙には影響しません。しかし、水に溶解すると、アンモニアは水酸化物イオンを生成し、リトマスの紙を青くします。
要約:
乾燥アンモニアガスは、その基本的な性質を示すために必要な条件がないため、Litmusの紙と相互作用しません。水に溶解すると、アンモニアは加水分解を受け、水酸化物イオンを放出します。これは、溶液の基礎性の増加により、リトマスの紙を青く変えます。