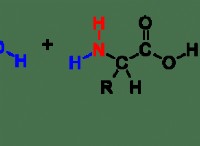
その理由は次のとおりです。
* 高い電気陰性度: フッ素は、すべての元素の中で最も高い電気陰性度を持っています。これは、電子に強い魅力を持っていることを意味します。
* 価電子: 各フッ素原子には7つの原子価電子があります。つまり、安定したオクテット(最も外側のシェルに8電子)を達成するにはもう1つの電子が必要です。
* 電子の共有: 安定性を達成するために、2つのフッ素原子が孤立した価電子を共有し、共有結合を形成します。この共有電子のペアは、原子を一緒に保持する両方の核に引き付けられます。
要約:
フッ素原子は、安定したオクテット構成を実現するために電子を共有し、強力な共有結合をもたらすため、分子(F₂)を形成します。この結合は、フッ素の高い電気陰性度によってさらに強化され、非常に安定した二原子分子につながります。