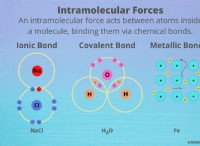
* 電子は結合を決定します: 原子をまとめて分子を形成する化学結合は、電子の相互作用によって形成されます。
* 価電子: 最も外側のシェル(価電子)の電子は、結合に最も関与するものです。価電子の数と配置は、原子が他の原子とどのように相互作用するかを決定します。
* 反応性: 多数の原子価電子を持つ原子は、反応性が低い傾向があり(たとえば、貴族)、原子がほとんどない原子はより反応的です(例:アルカリ金属)。
陽子と中性子は原子のアイデンティティ(原子数と質量)にとって重要ですが、それらはその化学的挙動に直接影響しません。
簡単なアナロジーは次のとおりです。小さな太陽系のような原子を考えてください。核(陽子と中性子)は太陽のようで、質量と安定性を提供します。電子は惑星のようなもので、核を周回し、原子が他の原子とどのように相互作用するかを決定します。