その理由は次のとおりです。
* イオン化合物は、静電引力によって形成されます: 陽イオン(正に帯電したイオン)と陰イオン(負に帯電したイオン)は、強力な静電力によって一緒に保持されます。
* 充電中立性: イオン化合物の全体的な電荷は中性でなければなりません。これを達成するには、陽イオンからの正の電荷の数は、陰イオンからの負の電荷の数のバランスをとる必要があります。
* 経験式: イオン化合物の化学式は、電荷の中性を満たすイオンの最も単純な全自由比を表します。
例:
塩化ナトリウム(NaCl)
*ナトリウム(Na)は+1カチオン(Na⁺)を形成します。
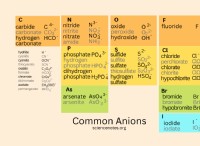
*塩素(Cl)は-1アニオン(Cl⁻)を形成します。
*電荷の中立性を達成するために、1つのナイオンが1つのcl clotionと結合され、式NaClが生成されます。
注:
イオン化合物の式は、結晶格子に存在する実際のイオン数を必ずしも表すものではありません。電荷の中立性を維持する最も単純な比率のみを表します。