その理由は次のとおりです。
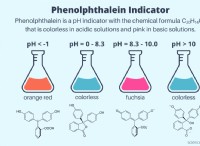
* 溶液中に水酸化物イオン(OH⁻)を生成します: 溶液中の水酸化アンモニウムは、わずかに解離し、アンモニウムイオン(NH₄⁺)と水酸化物イオン(OH⁻)を産生します。水酸化物イオンの存在は塩基の特徴です。
* 酸と反応して塩と水を形成する: 他の塩基と同様に、酸を中和し、塩と水を形成することができます。たとえば、塩酸(HCl)と反応して、塩化アンモニウム(NH₄Cl)と水(H₂O)を産生します。
重要な注意: 水酸化アンモニウムは多くの場合、用語として使用されますが、純粋な水酸化アンモニウムは不安定であり、別の化合物として存在しないことを理解することが重要です。一般に「水酸化アンモニウム」と呼ばれる溶液は、実際にはアンモニアの水溶液です(NH₃)。
この溶液中のアンモニア分子は、水分子と反応して、少量のアンモニウムイオン(NH₄⁺)と水酸化物イオン(OH⁻)を形成し、溶液を基本にします。