フェノールフタレイン指示薬は、酸性および強アルカリ性条件下で無色、常アルカリ性条件下でフクシアピンク色を呈するpH指示薬溶液です。ここでは、さまざまな pH 範囲での色、色の変化の化学、フェノールフタレイン指示薬の作り方、および化学物質の用途について説明します。
フェノールフタレインの pH 範囲と色
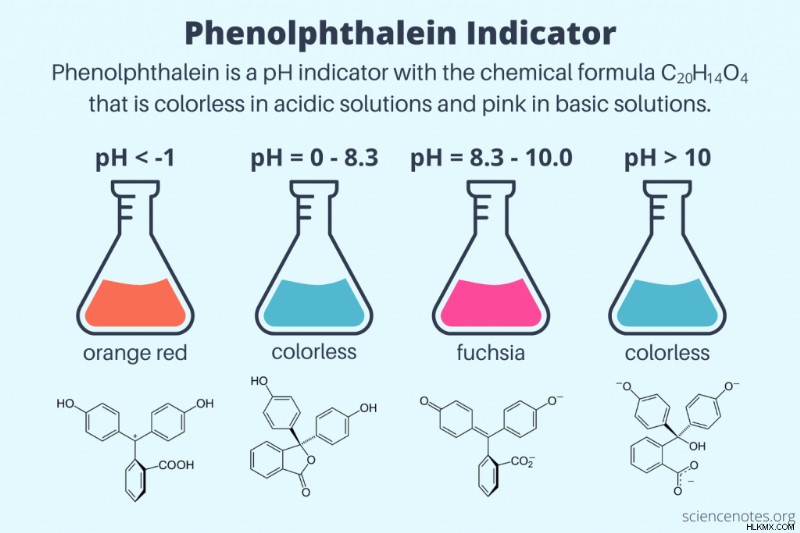
フェノールフタレインの 2 つの主な色は、指示薬の濃度に応じて、無色とピンク紫赤のフクシアです。フェノールフタレインは、酸性、中性および弱塩基性条件下で無色です。 pH 値が 8.3 から 10.0 の間ではピンク色で、pH 値が 10 を超えると再び無色になります。濃硫酸のように極端に低い pH では、色は橙赤色に変わります。ただし、すべての強酸で橙赤色が見られるわけではありません。
| 種 | H3 で | H2 で | で | In(OH) |
| pH | <1 | 0-8.3 | 8.3-10.0 | >10.0 |
| 条件 | 強酸性 | 酸性または中性 | 基本 | 基本的なこと |
| 色 | オレンジ | 無色 | パープルピンク | 無色 |
水溶液中のフェノールフタレインには、少なくとも 4 つの状態があります。極端な酸性条件下では、指示薬はオレンジ色のプロトン化された形 (HIn) になります。強酸性、中性、弱アルカリ性の条件下では、無色のラクトン体(HIn)を呈します。紫がかったピンク色は、フェノール (In) の二重脱プロトン化またはアニオン形態が優勢な塩基性条件下で形成されます。アルカリ度が上昇すると、指示薬が In(OH) 型に変換されるため、色はゆっくりと薄くなります。
フェノールフタレイン指示薬溶液の作り方
あらかじめ混合されたフェノールフタレイン指示薬溶液を購入できますが、自分で簡単に準備できます。フェノールフタレインは水にいくらか溶けますが (400 mg/L)、エタノールまたはエーテルによく溶けます。したがって、通常、最初に粉末の染料をアルコールに溶かしてから水で希釈するか、50% のアルコールに溶かします。
1% フェノールフタレイン指示薬溶液のレシピは次のとおりです:
<オール>別の一般的な定式化は 0.5% 溶液です:
<オール>フェノールフタレインの用途
フェノールフタレイン指示薬の最も一般的な用途の 1 つは、酸塩基滴定の終点を見つけることです。ただし、この化学物質には別の目的があります。
- 酸塩基滴定用pH指示薬
- コンクリート炭酸化の pH インジケーター
- 消えるインク
- 「ハリウッド ヘア」バービーなどの色が変わるおもちゃ
- 色付きの泡
- 下剤:下剤としてのフェノールフタレインの使用は、発がん性の可能性があるため、大部分が中止されました。
- フェノールフタレインの還元型であるフェノールフタリンは、血液の Kastle-Meyer テストで使用されます。
- フェノールフタレインは万能指示薬の成分です。
参考文献
- Dunnick, J.K.;ヘイリー、JR (1996)。 「フェノールフタレインへの暴露は、実験モデル系で複数の発がん性効果を引き起こします。」 がん研究 . 56 (21):4922–4926.
- シュヴァルツェンバッハ、ジェロルド (1957)。 複合滴定 .ハリー・アーヴィング訳(第1英語版)。ロンドン:Methuen &Co.
- ウィトケ、ゲオルク (1983)。 「さまざまな pH 値でのフェノールフタレインの反応」。 Journal of Chemical Education . 60 (3):239. doi:10.1021/ed060p239
- Zumdahl, Steven S. (2009). 化学原理 (第6版)。ニューヨーク:ホートン ミフリン カンパニー