希釈原理
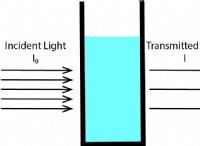
溶液を希釈すると、溶質の量(この場合はHCl)を同じように保ちながら、溶媒(水など)を追加します。 溶質のモルは一定のままですが、体積は増加し、濃度が低くなります(臼歯)。
計算
1。 Hclのモル:
- 初期濃度(0.125 m)と体積(100 mL =0.1 L)から始めます。
-hcl =モル××体積のモル=0.125 mol/l×0.1 l =0.0125モル
2。最終モル濃度:
- 現在、HCl(0.0125モル)のモルは、新しいボリューム(250 mL =0.25 L)に溶解します。
- 最終モル=HCl /最終体積のモル=0.0125モル / 0.25 L = 0.05 m
したがって、結果の溶液の臼歯は0.05 mです。