* 電子構成: 水素には1つのプロトンと1つの電子しかありません。 ヘリウム(2つの電子を持つ)のような安定した高貴なガス構成を実現するには、別の電子を獲得する必要があります。
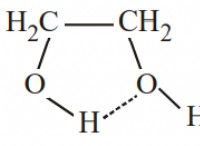
* 共有結合: その電子を別の水素原子と共有することにより、両方の原子が安定した構成を実現します。この共有電子ペアは、共有結合を形成し、H₂分子を作成します。
* 強い結合: H₂分子は強力な共有結合によってまとめられており、水素がこの珪藻形に存在するためにエネルギー的に好ましいものにします。
なぜ一酸化類はしませんか?
* 不安定な構成: 単一の水素原子(H)は、対応のない電子を持ち、非常に反応性と不安定にします。外側のシェルを完成させるために絆を形成することを容易に求めます。
* エネルギーに関する考慮事項: H₂分子の形成はエネルギーを放出し、個々の原子よりも安定しています。
例外:
* 高温: 極端に高温では、H₂分子は運動エネルギーの増加により、個々の水素原子に分解される可能性があります。
* プラズマ: プラズマ状態では、水素は主にイオン(H⁺)および電子として存在します。
要約すると、水素の二原子形態は、その電子構成、共有結合によって得られた安定性、および結合形成に関連するエネルギー放出の結果です。