その理由は次のとおりです。
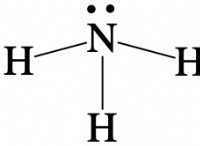
* 中央原子: 硫黄は中心原子です。
* 価電子: 硫黄には6つの原子価電子があり、各塩素(Cl)原子には7があります。
* 結合: 硫黄は、その原子価電子の2つを使用して、2つの塩素原子を持つ単一結合を形成します。
* 孤立ペア: 硫黄には残りの2つの原子価電子があり、孤独なペアを形成します。
硫黄原子にこの孤立したペアが存在すると、2つの塩素原子が互いに近づき、曲がったりV字型のジオメトリを押し出したりします。
VSEPR理論(価数シェル電子ペア反発)を使用して、中心原子の周りの電子ペアの配置に基づいて分子の分子形状を予測できます。